Das Wichtigste verständlich
| Die Helicobacter-Gastritis (kurz Hp-Gastritis) ist eine Entzündung des Magens durch die Infektion mit dem Magenkeim Helicobacter pylori (Hp). Sie geht unbehandelt in eine chronische Verlaufsform über und gilt als Risikofaktor für Magenkrebs, ein Magenlymphom und auch für weitere Erkrankungen, wie eine Arteriosklerose. Eine Hp-Besiedlung der Magenschleimhaut sollte daher erkannt und behandelt werden. Die Infektion erfolgt oral-oral oder fekal-oral meist bereits in der Kindheit. Symptome: Das akute Stadium ist durch mehr oder weniger heftige Übelkeit und Brechreiz charakterisiert; es wird oft als „Magenverstimmung“ empfunden und später nicht mehr erinnert. Im chronischen Stadium können die Symptome völlig verschwinden, oder es können unspezifische Oberbauchbeschwerden (Dyspepsie) entstehen. Komplikationen: Zu den schwerwiegendsten Folgen und Komplikationen gehören das Magen- und Zwölffingerdarmgeschwür und der Magenkrebs. Assoziationen: Es besteht eine Assoziation einer Helicobacter-Infektion mit der Arteriosklerose, dem Glaukom, der Migräne und der Präeklampsie. Sie sollten sie bei der Diagnostik mit berücksichtigt werden – bzw. umgekehrt: wenn sie vorliegen, sollte nach einer Helicobacter-Infektion gesucht werden. Diagnostik: Die Erkennung sowohl einer Gastritis als auch einer Helicobacter-Infektion der Magenschleimhaut erfolgt zuverlässig durch die Histologie. Sie wird durch eine Magenspiegelung gewonnen. Die Besiedlung der Magenschleimhaut mit Helicobacter-Keimen kann durch eine chemische Reaktion in einem Schnelltest noch während einer Magenspiegelung entdeckt werden. Therapie: Die Behandlung stützt sich auf eine Kombination von Antibiotika und Säureblocker (Hemmer der Magensäureproduktion). Wegen der möglichen Entwicklung von Resistenzen der Keime gegen verschiedene Antibiotika, sind ausgeklügelte Therapie-Regime erforderlich. Prognose: Die chronische Verlaufsform einer Hp-Gastritis führt zu einer Schleimhautatrophie (Abnahme von Drüsen, Vermehrung von Fasern, Epithelmetaplasie: chronisch atrophische Gastritis) und beinhaltet ein erhöhtes Risiko eines Magentumors (Magenkrebs, Magenlymphom). In Ostasien ist das Risiko von Magenkrebs ausgeprägter als in westlichen Ländern. Die Reinfektionsrate nach Eradikation (Auslöschung) der Magenkeime ist gering. → Helicobacter pylori |
Entstehung
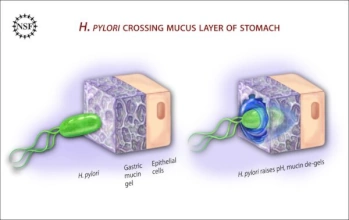
Die Helicobacter-pylori-Gastritis, kurz Hp-Gastritis wird durch das Gram-negative und obligat pathogene Bakterium Helicobacter pylori (H.p.) ausgelöst und unterhalten 1. Die Infektion erfolgt über eine orale Aufnahme (oral-oral, fekal-oral). Von Helicobacter pylori (Hp) wird das Enzym Urease (ein Harnstoff-spaltendes Enzym) in großen Mengen gebildet. Das entstehende Ammonium verbessert die pH-Bedingungen für eine Hp-Kolonisierung der Magenschleimhaut. 2 3
Undichtigkeit der Schleimhaut: Durch die Magenkeime wird die Dichtigkeit der Magenschleimhaut (durch Schädigung der tight junctions) gestört. Es entsteht initial eine akute Gastritis. Histologisch finden Helicobacter-Bakterien in der Schleimhaut, wobei das Bakterium spezifisch im Bereich des Magenepithels (nicht im Bereich intestinaler Metaplasien) gefunden wird (Gewebstropismus). Helicobacter wird auch in Magenschleimhautinseln im Bulbus duodeni gefunden, wo der Keim an der Entstehung eines Zwölffingerdarmgeschwürs beteiligt ist 4.
Muzine: Die Lipopolysaccharide von Helicobacter pylori ähneln denen der Lewis-Blutgruppen-Oberflächenantigene der gastralen Mukosazellen. Daher wird vermutet, dass die Magenkeime eine Immuntoleranz hervorrufen, welche das Überleben der Keime fördert. 5 6 Verschiedene Muzine mit veränderten Sialylierungsmustern können sich in ihrer Schutzwirkung gegen Säure und Pepsin unterscheiden, was zu unterschiedlichen Schleimhautreaktionen auf einen Hp-Befall führen kann 7.
Das Immunsystem des Körpers wird durch die Keime in seiner Reaktivität verändert. 8 Es nehmen Infiltrationen in der Schleimhaut mit Immunzellen (Lymphozyten) zu. Sie setzen autoimmunologische Mechanismen in Gang, bei denen Antikörper gegen Helicobacter pylori gebildet werden, die mit Schleimhautantigenen kreuzreagieren, also die Schleimhaut mit angreifen. Dies soll die im Laufe der Zeit entstehende Atrophie mit Abnahme der Drüsen und der Säurebildung (Hypochlorhydrie) erklären 9. Während der Entwicklung zu einer atrophen Schleimhaut nimmt die Helicobacter-Besiedlung ab, sodass im Endzustand einer atrophischen Gastritis kaum noch oder keine Hp-Besiedung mehr nachweisbar ist 10.
Risiko Tumor- und Ulkusbildung: Die Kolonisation bzw. Infektion der Magenschleimhaut mit Helicobacter bedeutet ein erhöhtes Risiko für peptische Geschwüre sowie für Adenokarzinome des Antrums oder Korpus 11 12 oder eines Magenlymphoms (MALT-Lymphom, B-Zell-Lymphom der Magenwand). Es gibt diverse Stämme mit unterschiedlicher Pathogenität. Die Stämme cagA+, vac s1, iceA1 sind in dieser Beziehung besonders pathogen. Das Magenkarzinomrisiko (Cardiakarzinome ausgeschlossen) ist bei Hp-Befall bis zu 150-fach höher als bei nichtinfizierten Personen. Das auf dem Boden einer Hp-Gastritis erhöhte Risiko für ein Magenkarzinom (ausgenommen für das Cardiakarzinom) ist pathogenetisch nicht vollständig verstanden. Das Risiko bleibt offenbar auch nach Eradikation von H.p. weiterhin erhöht. 13
Symptomatik und Verlauf
Akute Phase: Nach Erstinfektion bzw. Inokulation des Magens mit Helicobacter pylori entwickelt sich eine akute Gastritis mit meist milden bis mäßigen, manchmal auch heftigen und krampfartigen epigastrischen Schmerzen, sowie Übelkeit und (seltener) Erbrechen. Gelegentlich verläuft eine Erstinfektion unbemerkt.
In ca. 80% wird die Infektion chronisch. Die meisten Menschen mit einer chronischen Infektion bleiben asymptomatisch. Einige entwickeln eine funktionelle Dyspepsie, d. h. unbestimmte Magenbeschwerden.
Chronsiche Phase: Bei jahrelangem Verlauf kann es zu Symptomen durch Folgen der sich entwickelnden chronisch-atrophischen Gastritis kommen. Die Schleimhautatrophie betrifft hauptsächlich den Corpus des Magens (i. G. zur Typ-A-Gastritis, bei der sie den Fundus des Magens betrifft). Sie ist mit einem erhöhten Krebsrisiko verbunden 14. Anhaltende Inappetenz, Völlegefühl und Übelkeit können durch eine chronische aktive Gastritis, aber auch durch ein Magenkarzinom bedingt sein.
Histologie
Epithelschädigung und entzündliche Infiltrate in der Lamina propria mit polymorphkernigen Granulozyten, Eosinophilen und Lymphozyten (dem Mukosa-assoziierten lymphatischen Gewebe (MALT) zugehörig, oft lymphoide Follikel in der Histologie). Im Laufe der Jahre entwickelt sich eine atrophische Gastritis (jährlicher Prävalenzanstieg um ca 1-3%), und es lassen sich zunehmend intestinale Metaplasien nachweisen. Beide Veränderungen erhöhen das Risiko der Entwicklung eines Magenkarzinoms.
Diagnostik
Unklare und anhaltende Magenbeschwerden werden am effektivsten durch eine Magenspiegelung (Gastroskopie) abgeklärt, vor allem wenn sich eine Gewichtsabnahme hinzugesellt. Es gilt eine Hp-Gastritis und einen Hp-assoziierten Tumor (Magenkarzinom, MALT-Lymphom, neuroendokrinen Tumor) rechtzeitig zu erkennen 15.
Bei der Magenspiegelung wird routinemßig eine Biopsie aus Antrum und Corpus entnommen und histologisch aufgearbeitet. Häufig wird parallel auch ein Urease-Schnelltest durchgeführt. Eine Endoskopie bei asymptomatischen Personen alleine zum Zweck eines Helicobacter pylori-Nachweises gilt als nicht indiziert.
Die Diagnostik einer Helicobacter-Gastritis stützt sich auf den direkten Nachweis des Bakteriums oder seiner Bestandteile oder Stoffwechselprodukte. Der Nachweis von Antikörpern im Wirt gegen Helicobacter ist nicht beweisend; Antikörper können längere Zeit nach Eradikation weiterhin nachweisbar bleiben.
- Histologischer Nachweis (PE bei Endoskopie): er gilt heute als Goldstandard für den Nachweis einer Helicobacter-Besiedlung der Magenschleimhaut. Die HE-Färbung ist geeignet zur Beurteilung des Gewebes und eines starken Helicobacter pylori-Befalls, die Silber-Färbung nicht zur Gewebsbeurteilung sondern nur des Helicobacter-pylori-Befalls (sensitiv), die Genta-Färbung lässt beides gut erkennen.
- Urease-Nachweis in einer Gewebeprobe (PE bei Endoskopie): dieser Schnelltest beruht auf einem Farbumschlag z. B. eines Agargelplättchens durch die Urease-Aktivität der Gewebsprobe. Antibiotika oder Protonenpumpenblocker (PPI) können zu falsch negativen Ergebnissen führen. Sensitivität und Spezifität > 90%. Dieser Test ist am günstigsten, wenn eine Gewebeprobe nicht histologisch untersucht werden muss.
- Harnstoff-Atemtest: markierter Harnstoff (13C oder 14C) wird bei Helicobacter pylori-Befall im Magen zersetzt; das entstehende markierte CO2 wird in der Atemluft gemessen (Massenspektrometrie bzw. Szintillationszähler nötig). Sehr aussagekräftige, nicht invasive Methode, aber wenig sensitiv bei geringem Befall. Sie eignet sich zur Therapiekontrolle.
- H. pylori-Stuhl Antigen-Test: scheint in seiner Empfindlichkeit und Aussage dem Harnstoff-Atemtest äquivalent zu sein; Sensitivität und Spezifität liegen bei 90%. Er weist eine aktive Infektion nach.
- PCR auf H.p.-DNA: dieser Nachweis ist zu 98% spezifisch. Er weist eine aktive Infektion nach.
- Helicobacter-Kultur: Sie ist spezifisch, aber aufwändig. In der Regel ist sie wegen der hohen Aussagekraft der Histologie und des Urease-Schnelltests nicht erforderlich und daher nicht gerechtfertigt. Sie wird meist nur zur Resistenztestung bei fehlgeschlagener Eradikation und weiterbestehender Symptomatik und nachweisbarer aktiver Gastritis durchgeführt.
Umgebungsuntersuchungen
Es sollte bei der Diagnostik berücksichtigt werden, dass eine Helicobacter-Infektion nicht nur mit einer Gastritis und dem Magenkrebs, sondern auch mit der Arteriosklerose 16, einem Glaukom 17, der Migräne 18 und der Präeklampsie 19 assoziiert ist.
Unter diesem Gesichtspunkt sollte bei positivem Helicobacter-Nachweis auch nach solchen Krankheiten gefahndet werden, und umgekehrt sollten solche Krankheiten nach einem Helicobacterbefall suchen lassen. Bei positivem Ergebnis wäre eine Eradikation anzuraten!
Risiko Magenkarzinom
Eine chronische Helicobacter-Infektion ist die häufigste Ursache eines Magenkarzinoms. 20 In Japan ist die schwere Helicobacter-assoziierte Gastropathie mit einem Risiko von etwa 3 % mit der Entwicklung eines Magenkarzinoms verbunden; Patienten mit Magenulcera bei Helicobacter-Infektion haben ein höheres Risiko, solche mit Duodenalulzera ein deutlich niedrigeres. 21 Der bakterielle Virulenzfaktor, der zu dem hohen Krebsrisiko führt, ist als CagA (Cytotoxin-assoziiertes Gen A) identifiziert worden. 22 In westlichen Ländern ist das Magenkrebsrisiko wegen dem Überwiegen anderer, weniger virulenter Helicobacterstämme (siehe hier) geringer.
Therapie
Ziel der Behandlung ist es, eine Eradikation zu erreichen, um Komplikationen und Folgen zu vermeiden und Symptome zu lindern. Um das Magenkrebs-Risiko zu senken, sollte die Behandlung frühzeitig einsetzen, um der Entwicklung einer Magenschleimhautatrophie und von intestinalen Metaplasien rechtzeitig vorzubeugen.
Es gibt absolute und relative Indikationen für eine Eradikations-Therapie. Zu den absoluten Indikationen zählen die frische Hp-Gastritis und das MALT-Lymphom.
Die Behandlung beinhaltet einen Protonenpumpenhemmer (PPI) und eine Kombination von 2 oder 3 Antibiotika, wobei Amoxicillin, Chinolone, Metronidazol, Makrolide und Rifampicin gängig sind. Gegen Clarithomycin und Metronidazol entsteht eine zunehmende Resistenz. Entsprechend gibt es eine Reihe von Kombinationen, die als Erstlinien- oder Zweitlinientherapie und als Reservetherapie vorgeschlagen werden.
→ Dazu siehe hier.
Es ist unsicher und umstritten, ob sich eine ausgeprägte chronische Schleimhautatrophie nach Eradikation wieder bessern kann 23.
Erneute Infektion nach erfolgreicher Eradikation
In einer Südkoreanischen Studie zwischen 2005 und 2016 wurde eine Reinfektionsrate von 3,06% pro Personenjahr festgestellt 24. In einer anderen Studie über einen Beobachtungszeitraum von 2017 – 2022 lag die Reinfektionsrate bei 3,7 %. In den ersten 24 Monaten lag sie bei 5,9 % pro Personenjahr und danach 2,0 % bis 2,4 % pro Personenjahr 25. In einer Publikation wurde der Verdacht geäußert, dass unter den „Reinfektionen“ sich viele Fälle einer nicht vollständigen Eradikation verbergen 26.
Prognose
Ein Helicobacter-Befall der Magenschleimhaut bedeutet ein erhöhtes Risiko für
- ein Magenulkus,
- ein Magenkarzinom und
- ein Magenlymphom.
Wegen der Epithelmetaplasien in einer chronisch-atrophischen Gastritis, die als Praekanzerose wirkt, sollte eine qualitativ hochwertige endoskopische Kontrolle alle 3 Jahre erfolgen 23.
Eine erfolgreiche Helicobacter-Eradikation senkt (laut einer japanischen Arbeit) das Langzeitrisiko für Magenkrebs (über einen Zeitraum von mindestens 10 Jahren). 27 Die Hp-Eradikation gilt als eine wichtige Präventionsmaßnahme. Die Mortalität sank einer Untersuchung zufolge durch eine Eradikation innerhalb von 2 Jahren um 39 %. 28
Risiko Refluxkrankheit
Da eine Helicobacter-pylori-Infektion zu einer chronischen Gastritis mit reduzierter Säureproduktion führt, wurde vermutet, dass eine Eradikation zu einer erneut höheren Magensäureproduktion und damit zu vermehrten Refluxbeschwerden führt. Dies ist jedoch offenbar nicht der Fall, so dass auch Refluxpatienten mit gleichzeitig vorliegender Helicobacter-Gastritis ohne erhöhtes Risiko einer Verschlechterung eradiziert werden können. 29
→ Auf facebook informieren wir Sie über Neues und Interessantes!
→ Verwalten Sie Ihre Laborwerte mit der Labor-App Blutwerte PRO – mit Lexikonfunktion.
Verweise
- Helicobacter pylori
- Helicobacter-Eradikation
- Gastritis
- Hp-Gastritis
- Erosive Gastritis
- Magenkarzinom
- MALT-Lymphom
- Der Gastrointestinaltrakt
- Die Speiseröhre (Ösophagus)
- Der Magen
- Gastritis – einfach erklärt
- Gastritis in Bildern
Weiteres
- Mediators Inflamm. 2022 Mar 8;2022:2944156. DOI: 10.1155/2022/2944156.[↩]
- Infect Immun 1995; 63: 1669-1673[↩]
- J Membr Biol. 2006;212(2):71-82[↩]
- Ann N Y Acad Sci. 1998 Nov 17;859:96-111. doi: 10.1111/j.1749-6632.1998.tb11114.x[↩]
- Glycobiology. 2009 May;19(5):453-61[↩]
- Curr Opin Gastroenterol. 2006 Jan;22(1):3-7[↩]
- World J Gastroenterol. 2014 Oct 28;20(40):14913-20. doi: 10.3748/wjg.v20.i40.14913[↩]
- Best Pract Res Clin Gastroenterol. 2007;21(2):237-59. doi: 10.1016/j.bpg.2007.01.001.[↩]
- Gastroenterology 1991; 101: 437-445[↩]
- Gastroenterology 1996; 110: 926-938[↩]
- NEJM 1991; 325: 1127-1131[↩]
- Lancet 1993; 341: 1359-1362[↩]
- Adv Med Sci. 2007;52:55-60[↩]
- J Environ Pathol Toxicol Oncol. 2018;37(3):241-259. DOI: 10.1615/JEnvironPatholToxicolOncol.2018026839.[↩]
- PLoS Pathog. 2017 Nov 2;13(11):e1006653. DOI: 10.1371/journal.ppat.1006653.[↩]
- He C. J Atheroscler Thromb. 2014 Oct 24.[↩]
- Glob J Health Sci. 2014 Sep 18;6(7 Spec No):38263[↩]
- World J Gastroenterol. 2014 Oct 28;20(40):14965-72[↩]
- Front Immunol. 2014 Oct 9;5:484[↩]
- Nat Rev Cancer. 2010 Jun;10(6):403-14. doi: 10.1038/nrc2857.[↩]
- NEJM 2001; 345: 784-789[↩]
- Sci Rep. 2019 Jan 10;9(1):38. doi: 10.1038/s41598-018-37095-4.[↩]
- Postgrad Med. 2022 Apr 13:1-6. DOI: 10.1080/00325481.2022.2063604[↩][↩]
- J Gastroenterol Hepatol. 2019 Oct;34(10):1696-1702. doi: 10.1111/jgh.14639.[↩]
- Helicobacter. 2024 Jan-Feb;29(1):e13036. doi: 10.1111/hel.13036[↩]
- Scand J Gastroenterol Suppl. 1996;215:96-104. PMID: 8722391[↩]
- J Gastroenterol. 2015 Jun;50(6):638-44. DOI: 10.1007/s00535-014-1004-5.[↩]
- Gut. 2020 Dec;69(12):2113-2121. DOI: 10.1136/gutjnl-2020-320839[↩]
- Gastroenterology 2001; 121: 1120-1126[↩]