Die Antibiotikaresistenz von Bakterien ist ein weltweites Problem in der Medizin. Sie gefährdet
- die Heilung bakterieller Infektionen,
- die Infektionsprophylaxe
- bei Schwerkranken,
- bei Immunschwäche,
- bei medizinischen Eingriffen, die unter Antibiotikaschutz durchgeführt werden müssen.
Zunehmend entstehen Resistenzen gegen multiple Antibiotika (Multidrugresistenz, MDR), die fatale, nicht mehr behandelbare Infektionen zur Folge haben. Beispiel sind MRSA (Methicillin-resistenter Staphylococcus aureus). Eine neue Perspektive besteht in der Entwicklung besonderer Bakteriophagen, welche in die Problemkeime eingeschleust werden können, die zu ihrer Abtötung führen (s. u.).
→ Zu Antibiotika siehe hier.
Inhaltsverzeichnis
- 1 Ursache
- 2 Ausbreitung resistenter Keime
- 3 Vermeidung einer Übertragung
- 4 Multiresistenz
- 5 Bedeutung für den Menschen
- 6 Rolle von Plasmiden
- 7 Beispiel MRSA-Infektionen
- 8 Beispiel Tuberkulose-Resistenz
- 9 Beispiel Malaria-Resistenz
- 10 Beispiel Campylobacter-Enteritis
- 11 Perspektive bei Antibiotikaresistenz: Bakteriophagen
- 12 Antibiotikatoleranz und -persistenz
- 13 Verweise
Ursache
→ Auf facebook informieren wir Sie über Neues und Interessantes.
→ Verwalten Sie Ihre Laborwerte mit der Labor-App Blutwerte PRO – mit Lexikonfunktion.
Ursache der Antibiotikaresistenz ist die genetische Anpassungsfähigkeit der Bakterien. Mutationen sind bei der den Bakterien eigenen hohen Zellteilungsrate (ca. alle 20 Minuten) häufig. Unter ihnen befinden sich gelegentlich auch solche, die zu einer Resistenz gegen ein Antibiotikum führen. Solche Mutanten setzen sich durch und verbreiten sich rasch. Wenn sie einem zweiten Antibiotikum über längere Zeit ausgesetzt werden, kann sich auch gegen dieses eine Resistenz ausbilden. So haben sich im Laufe der letzten Jahrzehnte multiresistente Keime gebildet, die mit den etablierten Antibiotika nicht mehr behandelt werden können.
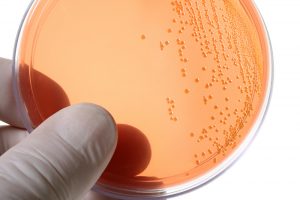
Förderlich für die Entwicklung einer Antibiotikaresistenz sind:
- Inadäquate Antibiotikatherapie beim Menschen
- unnötige Antibiotikatherapie, z. B. bei einem Virusinfekt oder bei einer lokalen offenen Entzündung ohne Keiminvasion,
- unzureichende Behandlung (zu kurz, zu geringe Dosierung),
- falsche Auswahl des Antibiotikums (nicht der Resistenzlage angepasst).
- Antibiotika in der Tierzucht (z. B. Rinder, Schweine, Hühnchen) zur Infektionsprophylaxe und Mastförderung. Es kommen verschiedene Wirksubstanzen zum Einsatz. Staphylokokken der Haut und Schleimhäute sind bei Tieren in Massenhaltungen multiresistent geworden (z. B. Stämme MRSA ST8, ST9, ST398) und besiedeln von dort den Menschen. Meist erkranken die Tiere in ihrer kurzen Lebenszeit bis zur Schlachtung nicht. Aber auch bei ihnen können schwer therapierbare Infektionen auftreten, beispielsweise eine Mastitis bei Milchkühen. (1)Lett Appl Microbiol. 2014 Dec;59(6):665-9
Eine weitere Hypothese der Entwicklung einer Antibiotikaresistenz besagt, dass Bakterien bereits vor Millionen von Jahren Gene hervorgebracht haben, die gegen natürlicherweise in der Natur auftretende Moleküle gerichtet sind, die als Signalstoffe wirken, aber in großen Mengen, die in der Natur nie vorkamen, auch antibiotisch wirksam werden. Diese natürliche Fähigkeit zur Antibiotikaresistenz sei in manchem Genom versteckt und würde durch den heutigen Antibiotikagebrauch demaskiert. (2)Front Microbiol. 2013 Mar 12;4:47 Dieser Hypothese entspricht die Beobachtung, dass subtherabeutische kleine Dosen von ß-Lactam-Antibiotika (wie Methicillin) die Biofilm-Bildung von MRSA (Wechsel in einen neuen Modus der Fortpflanzung als Zellaggregate auf Oberflächen) induziert, was nicht-ß-Lactam-Antibiotika nicht tun. (3)Dose Response. 2013 Jul 25;12(1):152-61 Je nach genetischer Ausstattung hemmen bestimmte Antibiotika die Biofilm-Bildung in einigen MRSA-Stämmen, so z. B. Rifampicin und Moxifoloxacin, die jedoch in anderen Stämmen eine Biofilm-Bildung hervorrufen. (4)Bratisl Lek Listy. 2014;115(8):483-6
Zum Seitenanfang und Inhaltsverzeichnis
Ausbreitung resistenter Keime
Die Ausbreitung der Faktoren, die für Virulenz, Resistenz und Immun-Escape mutierter Bakterienstämme verantwortlich sind, geschieht durch
- Zellteilung der Bakterien; Tochterzellen sind ebenfalls resistent: vertikale Ausbreitung der Resistenz),
- Übertragung von einem resistenten auf ein nicht resistentes Bakterium über Plasmide (freie DNA als mobile genetische Elemente) und Bakteriophagen (Viren, die Bakterien befallen). (horizontale Ausbreitung der Resistenz). (5)PLoS One. 2011 Mar 3;6(3):e17549
Die horizontale Übertragung geschieht, wie an MRSA festgestellt, sehr effektiv innerhalb weniger Stunden (6)Genome Biol Evol. 2014 Sep 25;6(10):2697-708 DOI: 10.1093/gbe/evu214.
Kläranlagen tragen zur Verbreitung der Gene für eine Antibiotikaresistenz bei, wobei Plasmide eine bedeutende Rolle spielen. (7)Front Microbiol. 2014 Oct 28;5:558
Die Übertragung von Tieren auf den Menschen geschieht überwiegend über Tierprodukte (Eier, Milch etc.), direkten Tierkontakt oder über Tierabsonderungen in die Umwelt (Urin, Feces, Speichel etc.). Die meisten Veterinärärzte sind positiv.
Zum Seitenanfang und Inhaltsverzeichnis
Vermeidung einer Übertragung
Eine Vermeidung einer Übertragung resistenter Keime von Tieren auf den Menschen scheint illusorisch zu sein.
MRSA werden von Mensch zu Mensch durch direkten Kontakt übertragen. Dies geschieht meist im Krankenhaus und in Pflegeheimen, u. a. auch über Pflegepersonal. Die Krankenhäuser unternehmen erhebliche Anstrengungen, die Ausbreitung durch Hygienemaßnahmen einzuschränken. Gelegentlich werden die Betreiber für die in ihren Einrichtungen erworbenen MRSA-Infektionen juristisch verantwortlich gemacht. Sie schützen sich dagegen vielfach durch eine Eingangsuntersuchung der Patienten sowie durch einen Test des betreuenden Personals (Abstriche am Haaransatz der Stirn und der Nasenschleimhaut). Die Händedesinfektion spielt eine zentrale Rolle. Sie wird indirekt über den Verbrauch an Antiseptika überprüft.
Multiresistenz
Beispiele für multiresistente Keime mit zunehmender klinischer Relevanz sind
- multiresistenter Staphylococcus aureus,
- multiresistente Escherichia coli inkl. EHEC,
- multiresistente Klebsiella pneumoniae,
- multiresistenter Pseudomonas aeroginosa,
- multiresistente Mycobacterium tuberculosis (Zunahme durch Zuwanderung aus Osteuropa, Problem der Langzeitisolierung bei offener Tuberkulose),
- multiresistenter Campylobacter,
- multiresistente Salmonellen,
- multiresistente Helicobacter pylori (Zunahme der Resistenz gegen Clarithromycin und Metronidazol, siehe hier),
- multiresistente Malariaerreger (Plasmodium falciparum, vivax, tertiana, ovale): in Ostasien ein zunehmendes Problem (siehe hier).
Die Mechanismen, die zu einer Resistenz gegen Antibiotika führen, sind sehr unterschiedlich und von der Art der Antibiotikawirkung abhängig.
Zum Seitenanfang und Inhaltsverzeichnis
Bedeutung für den Menschen
Die Auswirkungen einer Multiresistenz von pathogenen Keimen beim Menschen sind unterschiedlich. In den vielen Fällen sind multiresistente Keime harmlose Kommensalen und besiedeln die Haut und Schleimhäute ohne Krankheitsauswirkungen. Dringen sie allerdings in den Körper ein, so ist ihre Krankheitswirkung abhängig von den Virulenzfaktoren der Bakterien. Keime, die zwar eine Multiresistenz, aber eine niedrige Virulenz aufweisen, sind weniger problematisch, als wenn ihre Virulenz hoch ist und sie Mechanismen haben, dem Immunsystem zu entkommen. Insbesondere auf Intensivstationen, auf denen sich abwehrgeschwächte Patienten befinden, sind multiresistente Keime ein außerordentliches Problem.
Rolle von Plasmiden
Die Antibiotikaresistenz von Bakterien kann auf zwei Wegen erworben werden: durch genetische Mutation und durch horizontale Ausbreitung über Plasmide. Plasmide sind nicht-chromosomale, freie zirkuläre DNA-Stränge, die genetische Informationen von Bakterium zu Bakterium („horizonal“) weitergegeben können. Sie werden als die wichtigsten Treiber der Ausbreitung resistenter Keime angesehen, und beschleunigen die Ausbreitung nosokomialer Infektionen in Krankenhäusern (8)Trends Microbiol. 2018 Dec;26(12):978-985. DOI: 10.1016/j.tim.2018.06.007, in Vogelschwärmen und in Tierzuchtanstalten. (9)Front Microbiol. 2022 Sep 29;13:969769. doi: 10.3389/fmicb.2022.969769
Zum Seitenanfang und Inhaltsverzeichnis
Beispiel MRSA-Infektionen
Penicillin wirkt vor allem gegen Gram-positive Mikroorganismen wie Streptokokken und Staphylokokken. Viele Bakterienstämme sind jedoch gegen Penicillin resistent geworden, weil sie den ß-Laktamring des Penicillins durch eine Penicillinase (eine ß-Lactamase) zu spalten vermögen und es damit unwirksam machen. Die ß-Lactamase wurde zuerst in Gram-negativen E. coli gefunden; sie „sprang“ in der aufkommenden Antibiotika-Ära durch Vektoren (Bacteriophagen und Plasmide) bald auch auf andere Bakterienarten über, so auch auf Staphylokokken. Um die Penicillinase-Resistenz bzw. ß-Laktamase-Resistenz der Bakterien zu überwinden, wurden neue Antibiotika entwickelt, so als erstes Methicillin und später Oxacillin. Die Bakterien jedoch entwickelten auch gegen diese Antibiotika Resistenzen. Die Folge sind nun multiresistente Keime, beispielsweise die klinisch relevanten multiresistenten Staphylokokken. MRSA bedeutet ursprünglich „Methicillin-resistenter Staphylococcus aureus“. Da MRSA meist gegen alle ß-Lactam-Antibiotika resistent sind und zudem meist auch gegen andere Antibiotikaklassen wie Chinolone, Aminoglycoside oder Erythromycin, wird die Abkürzung oft auch als „multiresistenter Staphylococcus aureus“ übersetzt. Für solche Keime kommen Reserveantibiotika, wie Vancomycin und Linezolid in Frage, sofern das Antibiogramm dies noch zulässt.
Beispiel Tuberkulose-Resistenz
Die Tuberkulosebakterien werden zunehmend gegen verschiedene Antibiotika resistent; es entwickelt sich eine multi-drug-resistente Tuberkulose (MDR-Tb). Meist beziehen sich die Resistenzen auf Isoniazid und Rifampizin. Typischerweise entstehen solche Resistenzen bei unzureichender Dosierung und Therapiedauer. Dabei spielen eine nur geringe Compliance der Patienten eine Rolle, die von sich aus die Medikamente absetzen, wenn es ihnen besser geht, wenn sie ihre Medikamente gelegentlich vergessen, aber auch wenn sie zu starke Nebenwirkungen verspüren. Es werden zunehmend Zweitlinienmedikamente erforderlich. Allerdings tauchen immer mehr Fälle einer extensiven Antibiotikaresistenz auf, die eine Therapie unmöglich erscheinen lässt (siehe hier).
Zum Seitenanfang und Inhaltsverzeichnis
Beispiel Malaria-Resistenz
Malaria ist eine Infektionskrankheit, die durch Einzeller (Plasmodien) und nicht durch Bakterien hervorgerufen wird. Dennoch sind die Mechanismen der Vorbeugung und Therapie ähnlich. Malaria hat als Risiko in tropischen Ländern erhebliche Bedeutung. Sie schien durch systematische Bekämpfung ausrottbar gewesen. Nun sind jedoch gegen Artemisinin, einem hoch potenten Antimalariamittel pflanzlicher Herkunft (ähnlich einem Antibiotikum gegen Bakterien) in Ostasien erneut Resistenzen aufgetreten, die nach derzeitigem Stand der Medikamentenentwicklung nicht suffizient behandelt werden können. Artemisinin war bereits ein Reservemittel, da die Plasmodien gegen die bisherigen Medikamente resistent geworden waren. Eine wirksame Prophylaxe bei Reisen in die betroffenen Ländern existiert nun nicht mehr (siehe hier).
Beispiel Campylobacter-Enteritis
Campylobacter-Bakterien (häufig C. jejuni, seltener C. coli) sind die häufigsten Erreger von Durchfallerkrankungen (Gastroenteritis) durch verdorbene Speisen. Solche Infektionen können mit verschiedenen Organbeteiligungen einhergehen, so beispielsweise mit einer reaktiven Arthritis oder Neuropathien. Häufige Ursache der Infektionen sind nicht hoch genug erhitztes Geflügel (z. B. Masthähnchen, die selbst nicht krank sind), und nicht pasteurisierte Milch. Meist sind die Erkrankungen selbstlimitierend und bedürfen keiner Antibiose. Bei schweren Verläufen gilt das Makrolid Erythromycin als Mittel der ersten und Chinolone wie Ciprofloxacin Mittel der zweiten Wahl, Tetracycline und Gentamycin Mittel der dritten Wahl. Die häufige und inadäquate Antibiotikatherapie und vor allem der Antibiotika-Einsatz in der Tierzucht hat seit Jahren zu einer zunehmenden Resistenz der Keime gegen selbst Antibiotika der dritten Wahl geführt (10)Emerg Infect Dis. 2001 Jan-Feb;7(1):24-34, die nun für tatsächliche Notfälle, z. B. bei Menschen mit Immunsuppression, nicht mehr immer zur Verfügung stehen können. (11)Biomed Res Int. 2013;2013:340605
Zum Seitenanfang und Inhaltsverzeichnis
Perspektive bei Antibiotikaresistenz: Bakteriophagen
Seit Jahrzehnten dreht sich eine Spirale aus Entwicklung neuer Antibiotika und Resistenzentwicklung der Bakterien. Problematisch wird die antibiotische Therapie erst, wenn Bakterien auch für die Reservemedikamente eine Resistenz entwickeln (s. o.).
Eine neue Entwicklung greift alte Ideen auf, die den Einsatz von Bakterophagen zur Bekämpfung von bakteriellen Infektionen propagierten. Dabei wird ausgenutzt, dass Bakteriophagen mit genetischer Information bepackt werden können, die den Keim, den sie befallen sollen, schwächen. So werden lytische Bakteriophagen entwickelt, die MRSA zerstören. (12)World J Gastrointest Pharmacol Ther. 2017 Aug 6;8(3):162-173. DOI: 10.4292/wjgpt.v8.i3.162 Wenn Phagen als Medikamente dienen sollen, müssen sie daraufhin untersucht werden, dass sie keine Resistenzgene, virulente oder zytotoxische Gene mit sich tragen. Ihre Immunogenität sowie ihre Wechselwirkung mit den Zellen des Patienten muss überprüft werden. (13)Biologics. 2022 Oct 6;16:173-186. DOI: 10.2147/BTT.S381237
Interesse an Bakteriophagen als Therapeutika besteht nicht nur in der Humanmedizin, sondern auch in der Veterinärmedizin und in der Landwirtschaft zum Schutz vor Pflanzeninfektionen. (14)Viruses. 2014 Jul 1;6(7):2551-70 In Tierversuchen konnte bereits vor Jahren nachgewiesen werden, dass inokkulierte Staphylokokken nach Injektion von antibakteriellen Phagen wirksam bekämpft werden konnten; 97% der infizierten Mäuse wurden geheilt. (15)Antimicrob Agents Chemother. 2007 Aug;51(8):2765-73 Polyvalente Bakteriophagen (P-27/HP) vermochten Staphylococcus-aureaus-Stämme, die menschliche Krankheiten auslösen, in Kulturen wirksam zu hemmen, so auch MRSA. (16)Curr Microbiol. 2011 Jan;62(1):255-60 Auch gegen andere multiresistente Bakterienarten werden polyvalente Phagen entwickelt, beispielsweise gegen Achromobacter-Stämme. (17)PLoS One. 2014 Jan 22;9(1):e86935 Erste Erfahrungen bei Erkrankungen von Tieren und Pflanzen, zeigen, dass eine Resistenzentwicklung ein wesentliches Hindernis ist. Sie kann u.U. durch Kombination verschiedener Phagen überwunden werden. Ein Cocktail aus 6 Phagen wurde zur Behandlung von vogelpathogenen Escherichia-coli-Infektionen in der Hühnerzucht verwendet. Während nur ein Phagenstamm zu Resistenzen führte, traten bei dem Mix keine Resistenzen auf. (18)Viruses. 2020 Dec 19;12(12):1470. doi: 10.3390/v12121470
Antibiotikatoleranz und -persistenz
→ Zur Antibiotukatoleranz und Antibiotikapersistenz siehe hier.
→ Auf facebook informieren wir Sie über Neues und Interessantes.
→ Verwalten Sie Ihre Laborwerte mit der Labor-App Blutwerte PRO – mit Lexikonfunktion.
Verweise
Zum Seitenanfang und Inhaltsverzeichnis
[vc_wp_search]
Literatur