Allgemeines
Die Hepatitis B ist eine Entzündung der Leber. Sie wird durch das Hepatitis-B-Virus (ein DNA-Virus, Abk. HBV) hervorgerufen und wird meist durch Sexual- und Blutkontakt übertragen. Alle Körperflüssigkeiten können das Virus enthalten.
In der Mehrzahl der Fälle verläuft die Hepatitis B akut und heilt aus. In 10 % verläuft sie unbemerkt oder nach unspezifischen Symptomen chronisch und kann in eine Leberzirrhose münden.
Bei chronischem Verlauf steigt das Risiko eines hepatozellulären Karzinoms (Leberkrebs). Bei chronischem Verlauf kommt eine virustatische Therapie in Betracht.
Eine Impfung gegen HBV ist eine wirksame Vorbeugung und wird bei erhöhtem Infektionsrisiko dringend empfohlen.
Epidemiologie
Häufigkeit: Weltweit gibt es schätzungsweise 257 Millionen HBV-Infektionen mit 887.000 Todesfällen. Todesursachen sind häufig eine Leberzirrhose und Leberkrebs (hepatozelluläres Karzinom, HCC).
Die Verbreitung (Prävalenz) ist regional sehr unterschiedlich: Südostasien > 8 % ; Ost- und Südosteuropa, Mittlerer Osten und Japan 2 – 7 %; Westeuropa und Nordamerika < 2 %. 1
Die HBV-Übertragung geschieht weltweit am häufigsten über eine Mutter-Kind-Transmission, vor allem während der Geburt, und dann von Kind zu Kind. In westlichen Ländern werden die meisten Infektionen im frühen Erwachsenenalter übertragen. Infektion sind vermehrt zu gewärtigen bei Menschen mit Polytransfunsionen, Hämophilie, Hämodialyse, häufig wechselndem Geschlechtsverkehr (HWG), intravenöser Drogenabhängigkeit sowie bei Bewohnern von Einrichtungen für geistig Behinderte.
Entstehung
Infektiöse und nicht-infektiöse Partikel
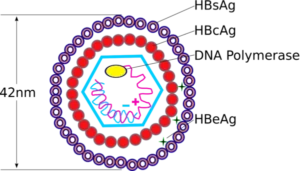
Im Serum von Hepatitis-B-Patienten befinden sich 3 verschiedene Partikel:
- sphärische Partikel,
- filamentöse Partikel, sie bestehen nur aus HBsAg (vormals als Australia-Antigen bezeichnet) und sind nicht infektiös,
- komplexe Strukturen „Dane-Partikel“ (Virionen, Hepadnaviren).
Das Verhältnis von HBsAg-Partikeln zu Dane-Partikeln beträgt etwa 1.000:1. Die Hepadnaviren infizieren verschiedenste Körperzellen, vor allem Hepatozyten, Zellen des hämatopoetischen Systems (Knochenmark, Milz, Lymphknoten), Thymus, Endothelzellen, Nieren, Pankreas (Bauchspeicheldrüse).
Entwicklung einer Leberentzündung
Das Hepatitis-B-Virus (HBV) ist ein nicht zytopathisches Virus (es schädigt die Leberzellen nicht direkt). Der Zelluntergang erfolgt durch Angriff des Immunsystems auf die befallenen Leberzellen: Lymphozyten greifen diejenigen Leberzellen (Hepatozyten) an, die an der Oberfläche die Virusfaktoren HBc und HBe exprimieren (Nukleokapsid) (cellmediated cytotoxicity). Die Virusantigene müssen in Nachbarschaft zu MHC-Klasse-1-Antigenen der Leberzellen liegen, die zwar normalerweise von Hepatozyten kaum gebildet werden, jetzt aber vermehrt an der Zelloberfläche erscheinen.
Die Leber reagiert auf die Infektion durch Bildung von Interferonen. Nach einer HBV-Infektion wird endogenes Interferon-alpha gebildet, woraufhin MHC-Klasse-1-Antigene exprimiert werden; gleichzeitig steigen die Transaminasen im Serum an. Interferone bewirken, dass
- die viralen Antigene vermehrt an der Oberfläche befallener Zellen präsentiert werden,
- die Virusreplikation gestört wird,
- noch nicht infizierte Zellen vor Infektion geschützt werden, (preventing reinfection during the lysis of infected hepatozytes),
- T-Zellen (killer cells) aktiviert werden, die die Virusantigen-präsentierenden Zellen angreifen und eine Auflösung (Zytolyse) über programmierten Zelltod (Apoptose) einleiten.
Diagnostik
Diagnostik bei Verdacht auf eine HBV-Infektion:
Der erste Verdacht auf eine virale Hepatitis wird häufig durch folgende Informationen hervorgerufen :
- Kontakt mit Infizierten,
- Zugehörigkeit zu einer Risikogruppe (Drogenabhängige, Promiskuität, HWG),
- zufällig entdeckte Erhöhung von Transaminasen,
- zufällig entdeckte Leberveränderung in der abdominellen Sonographie der Leber.
Sicherung der Diagnose:
Die Diagnostik der Hepatitis B stützt sich wesentlich auf den Nachweis von Bestandteilen des Virus und seiner Genprodukte (HBsAg, HBeAg, HBcAg) und dem Nachweis der Wirtsreaktion (Anti-HBs, Anti-HBe, Anti-HBc). Als Screening auf eine möglicherweise vorliegende aktuelle Hepatitis-B-Infektion dient der Nachweis von HBsAg. Anti-HBc (global IgG und IgM) dient der Überprüfung einer Durchseuchung und weist nach, ob Kontakt mit dem Hepatitis-B-Virus (HBV) stattgefunden hat. Der Parameter alleine kann nicht unterscheiden, ob die Infektion floride ist, schwelt oder durchgemacht wurde. Anti-HBc-IgM deutet auf eine frische HBV-Infektion; es ist die erste Wirtsantwort.
Bei chronischer Hepatitis B wird eine PCR (polymerase chain reaction) zur Bestimmung der Viruslast durchgeführt. Eine Last von über 2000 IU/ml (entspricht dem alten Maß von etwa 10 000 Kopien/ml) ist im Zusammenhang mit erhöhten Transaminasen eine Behandlungsindikation.
Die okkulte Hepatitis
Sie verläuft unerkannt und ist ein epidemiologisches und ein diagnostisches Problem. Sie kann zwar ausheilen, sich aber auch zur Leberzirrhose weiterentwickeln. Zum Verdacht auf eine okkulte Hepatitis B führt der Befund von
- positivem Anti-HBc bei negativem HBs-Ag.
Wenn die daraufhin durchgeführte PCR den Nachweis von DNA des Hepatitis-B-Virus ergibt, wird von einer „okkulten HBV-Infektion“ (OBI) gesprochen 2.
→ Hepatitis B Diagnostik
→ Hepatitis-Serologie
Klinisches Bild
Allgemein
Die Symptome einer frischen HBV-Infektion können sehr unterschiedlich sein. Führend sind eine Gelbsucht und eine Abgeschlagenheit. Weitere Symptome und Befunde sind sehr variabel.
Symptome durch zirkulierende Immunkomplexe (ähnlich der Serumkrankheit) sind Fieber, Gelenkbeschwerden, Urtikaria, papulöse Akrodermatitis, Glomerulonephritis.
Symptome und Befunde durch vorübergehende Knochenmarkssuppression sind eine gemischte Kryoglobulinämie (Kälteantikörper im Blut) und eine Periarteriitis nodosa (50 % der Patienten mit P. n. sind HBsAg-positiv!).
Neugeborene und Kleinkinder
Der Verlauf ist häufig asymptomatisch und mündet in einen HBV-Carrierstatus oder eine Chronifizierung. Etwa 25 % sterben an den Folgen. (800.000 Geburten/Jahr in Deutschland, davon 6.500 von HBsAg-positiven Müttern; das Infektionsrisiko beträgt bis 90 %, dazu siehe hier).
Erwachsene
Bei Erwachsenen verläuft eine Hepatitis B meist akut; sie heilt in 90% aus. In 10% verläuft sie chronisch.
Schwangerschaft
Alle Schwangeren sollten auf HBsAg untersucht werden. Bislang wurde bei positivem Befund eine Entbindung durch Sektio empfohlen. 3 Direkt nach der Geburt beim Kind kombinierte aktive und passive Impfung zur Vorbeugung einer chronischen Hepatitis B, für den Fall einer perinatalen Infektion. Heute kann durch eine vorbeugende antivirale Behandlung mit Tenofovir-Alafenamidfumarate (TAF) die Mutter-Kind-Transmission praktisch auf Null gesenkt werden. 4
AIDS
Etwa 90 % der HIV-Infizierten haben Marker einer B-Hepatitis, die im Stadium des AIDS häufiger (etwa 25%) in eine chronische Hepatitis mündet. Sie verläuft trotz gesteigerter Virusreplikation (erhöhte HBeAg und HBV-DNA) meist milder. Es existiert ansonsten kein Unterschied zum Verlauf der akuten Hepatitis B. Die Hepatitis B beschleunigt den Verlauf des AIDS nicht. Im HIV-Infektionsstadium vor AIDS (wenn noch Immunkompetenz vorliegt, Zahl der Helferzellen >400/µl) sollte bei HBsAg- und AntiHBc-Negativität gegen Hepatitis B geimpft werden (in 4 Schritten zu den Zeitpunkten 0 und den Monaten 1, 2 und 6).
Verlauf
Der Verlauf einer Hepatitis B kann sehr unterschiedlich sein. Er variiert von einer inapparenten, anikterischen Infektion bis hin zum fulminanten Verlauf. Wenn die Transaminasen in der akuten Phase sehr stark erhöht sind, ist die Wahrscheinlichkeit für eine Ausheilung hoch. Wenn sie dagegen in einem niedrigen bis mittleren Bereich liegen, mündet die Erkrankung meist in einer chronischen Hepatitis (5-10%). Infektionen mit einer Präcore-Mutante und Superinfektionen mit Hepatitis B verlaufen häufiger progredient (siehe hier).
Patienten mit HBV-Infektion und normalen Transaminasen haben wahrscheinlich eine Immuntoleranz und einen benignen Verlauf ohne wesentliches Zirrhoserisiko.
Akute Hepatitis
Nach einer Inkubationszeit von 25 – 160 Tagen (durchschnittlich 75 Tage) kommt es zu einer akuten Leberentzündung mit unterschiedlich stark ausgeprägter klinischer Symptomatik (Gliederschmerzen, allgemeine Abgeschlagenheit, Ikterus), die sich meist nach 3 – 6 Wochen zurückbildet.
Andere Entwicklungsmöglichkeiten sind die fulminante Hepatitis mit Leberversagen, die chronische Hepatitis und die Entwicklung einer Leberzirrhose.
Chronische Hepatitis
In 5-10% der Fälle kommt es zu einer Chronifizierung. Davon sterben 50% vorzeitig durch die chronisch-entzündliche Lebererkrankung oder durch ein hepatozelluläres Karzinom (HCC). Neugeborene bekommen bei einer Infektion (vertikale Transmission) in 90 % einen Carrier-Status (Infektiosität ohne selbst krank zu sein), Erwachsene in 1 – 5 % (bei Männern 6 mal häufiger als bei Frauen).
Bei einem akuten Verlauf erreichen die Transaminasen i. d. R. Werte von über dem 50-fachen der oberen Normgrenze. In diesen Fällen ist eine Ausheilung wahrscheinlich. Je geringer die Transaminasen in der akuten Phase der Hepatitis ausfallen, desto höher ist das Risiko einer fehlenden Elimination von HBV nach 6 Monaten. Ab einer Laufzeit von 6 Monaten wird Chronizität angenommen. Bleiben die Transaminasen bei Werten unter etwa dem 20-fachen der oberen Normgrenze, so ist die Wahrscheinlichkeit eines chronischen Verlaufs hoch.
Chronische Verläufe entwickeln sich gehäuft bei Immungeschwächten, unter immunsuppressiver Therapie, bei Menschen mit Hypo- oder Agammaglobulinämie, Leprakranken und Patienten mit Down-Syndrom.
Chronizität (Viruspersistenz) kommt dann zustande, wenn
- das eigene Interferonsystem nicht ausreichend funktioniert,
- das zelluläre Abwehrsystem (natürliche Killerzellen und zytotoxische T-Lymphozyten) die antigenexprimierenden Hepatozyten nicht eliminieren,
- das humorale Abwehrsystem (mit Anti-HBs) die immer wieder frei werdenden Viren (bei Zytolyse) nicht abfangen und neutralisieren können.
Fibrosierende cholestatische Hepatitis
Sie kommt nach Lebertransplantation und Reinfektion des Transplantats vor, jedoch auch nach Knochenmarktransplantation. Bei dieser Form spielt möglicherweise eine Virusmutante eine Rolle, die direkt zytotoxisch ist.
Fulminante Hepatitis
Bei etwa 1 % der HBV-Infizierten tritt ein fulminantes Leberversagen auf.
Etwa 50 % der Patienten mit fulminantem Verlauf sind HDV koinfiziert und meist intravenös Drogenabhängige.
Therapie
Funktionelle Heilung
Heute ist eine „funktionelle Heilung“ in vielen Fällen erreichbar. Eine HBsAg-Seronegativität wird bei 3%-5% der Patienten nach einer 10-jährigen Therapie mit Nukleos(t)ide-Analoga gefunden. Bei 8%-14% der Patienten 3-5 Jahre tritt sie nach einer 48-wöchigen Behandlung mit pegyliertem Interferon ein. 5
Therapieoptionen
Ob und welche Therapie im Einzelfall in Frage kommt, hängt von den individuellen Bedingungen ab. 6 Folgende Möglichkeiten können erwogen werden :
- Bei der akuten Hepatitis B: es reicht eine symptomatische Therapie. Eine virustatische Behandlung ist bei einer hoch akut verlaufenden Hepatitis B nicht erforderlich, da sie meist ausheilt.
- Bei schweren Fällen mit Arteriitis Plasmapherese, bei akuter Glomerulonephritis kommt die Gabe von Lamivudin oder Interferon-alpha (IFN-alpha) infrage.
- Bei einer fulminanten Hepatitis mit Leberzerfall kommt eine Transplantation in Betracht (niedrige Reinfektionsrate).
- Bei fehlender HBV-Elimination nach 6 Monaten kommen Antimetabolite und Interferon (s. u.) in Betracht.
Therapie bei Hepatitis B mit einer Laufzeit > 6 Monate
Bei einer Laufzeit von über 6 Monaten müssen aufgrund der Persistenz der in den Zellen integrierten Virus-DNA Virustatika dauerhaft verabreicht werden. Anhaltend erhöhte Transaminasen (> 2-fach) bei einem Virusload von >2000 IU/ml sollten Indikation einer Behandlung sein. Ziel ist eine Reduktion der Symptomatik und der Langzeitfolgen. Die empfohlenen Therapieschemata umfassen Nukleos(t)id-Analoga (NAs) und Interferon bzw. pegyliertes Interferon. Pegyliertes Interferon hat den Vorteil einer dauerhafteren Reaktion und des Fehlens einer Virusresistenz. Eine anhaltende Reaktion auf Interferon allein wird jedoch nur bei einer Minderheit der Patienten erreicht. Daher wird i.d.R. eine Kombinations- oder sequenziellen Behandlung empfohlen. 7 8
Gründe einer fehlenden Heilbarkeit
Die Hepatitis-B-Therapie führt aus verschiedenen Gründen nicht zu einer völligen Viruselimination 9 :
- Versagen der Entfernung der kovalent geschlossenen zirkulären DNA (cccDNA: virale „covalently closed circular DNA“),
- Auftreten von Resistenzen,
- viraler Rebound ausgehend von latenten episomalen cccDNA-Reservoiren () nach Beendigung der Therapie,
- Nicht-Compliance des Patienten,
- Entwicklung von Escape-Mutanten der Viren.
Ein vielleicht erreichbares Ziel kann eine (trotz Persistenz von HBsAg im Serum) vollständige Unterdrückung der Virusreplikation sein. Sie wird als teilweise Heilung bezeichnet. Dazu sind verschiedene Entwicklungen im Gange (s.u.). 8
Erfahrungen
Sie betreffen hauptsächlich eine Behandlung mit Lamivudin oder Interferon-alpha (IFN) besonders bei HBeAg-Positivität, die eine hohe Replikationsrate des HB-Virus anzeigt. Bei 25-50% kann mit Interferon-alpha (5-10 MIU 3x/Woche für 4-6 Monate) eine Remission mit Serokonversion von HBeAg zu Anti-HBe erzielt werden (zuerst wird HBeAg später auch HBsAg negativ). Die Genotypen A und B sprechen besser an als C und D. Eine längere und intensivere Therapie kann die Serokonversionsrate bis auf 90% erhöhen, wobei jedoch nach Absetzen der Therapie Relapse häufig sind. Eine sequentielle Therapie mit zunächst Lamivudin (100 mg /d für 52 Wochen) gefolgt von IFN 5 MIU /d für weitere 16 Wochen nach den ersten 8 Wochen zeigte in einer Studie eine Verbesserung bezüglich Normalisierung der GPT, einer anhaltenden Serokonversion und einem HBV-DNA-Verlust. Nach Beendigung der Behandlung bekamen im Beobachtungszeitraum 80% der Patienten keinen Relaps (gegenüber 20% in der nur mit Lamivudin behandelten Gruppe). 10
- Lamivudin (Nukleosidanalogon) wird relativ gut vertragen und als „first-line-Therapie“ diskutiert, es führt häufiger zu einer Serokonversion (17 %, spontan ca 6 %) und scheint auch vor verstärkter Fibrosierung zu schützen. Allerdings treten schon nach 6-9 Monaten gehäuft Resistenzen auf (YMDD-Mutationen); nach 4 Jahren betreffen sie etwa 2/3 der Patienten. Hochreplikative HBeAg-Minusvarianten sprechen gut an, bedürfen aber wegen Relapsneigung offenbar einer Langzeittherapie.
- Langzeiterfolg einer IFN / Lamivudin-Therapie: Nach Serokonversion durch die Therapie bei chronischer Hepatitis B (HBeAg negativ, Anti-HBeAg positiv) kommt es häufig zu einem Relaps. In einer Studie betrug die Rate erneuten HBeAg-Nachweises nach Lamivudin allein 54%, nach Interferon-Therapie allein 32 % und nach einer Kombinationstherapie von Interferon und Lamivudin 23%. 11
Weitere Nucleotid/Nucleosidanaloga
- Adefovir (Nukleotidanalogon) steht als Therapiealternative zur Verfügung, wenn eine Resistenz gegen Lamivudin eintritt. 12 Selbst hat es eine Resistenz nach 5 Jahren von 29 % und keine Kreuzresistenz zu Lamivudin, so dass es in Kombination eingesetzt werden kann.
- Telbivudin (Präparat Sebivo, 600 mg/d) hat einen sehr guten Effekt auf die Virusreplikation 13, hat noch eine gute Resistenzlage (18% nach 2 Jahren), wird in der Regel sehr gut vertragen und gilt inzwischen ebenfalls als Erstlinientherapeuticum. Es ist dem Adefovir bezüglich HBV-DNA-Suppression bei chronischer Hepatitis B überlegen; in Woche 24 waren in der Telbivudin-Gruppe 39 % PCR-negativ vs. 12% in den Adefovir-Gruppen. 14
- Entecavir wirkt in Studien vielfach bei Patienten, die gegen Lamivudin resistent geworden sind, weniger gut bei solchen, die auch gegen Adefovir resistent sind. Auch dieses Nucleosidanalogon gilt als eine First-line-Therapieoption mit ähnlicher Wirksamkeit wie Telbivudin. 15 Entecavir kommt als Medikament bei Lamivudin-Resistenz und bei Immunsupprimierten in Frage, bei denen es Effektivität und gute Verträglichkeit gezeigt hat. 16
Vergleich der antiviralen Therapeutika bei HBeAg-negativer Hepatitis B
Entecavir erwies sich in einer vergleichenden Untersuchung bei mittlerer Belastung mit HBV-DNA potenter als eine Monotherapie mit Lamivudin, Adefovir oder Telbivudin. 17
Wirksame Therapie bedeutet gleichzeitig eine HCC-Prophylaxe
Die Behandlung mit Nucleosid-/Nucleotid-Analoga senkt das Risiko der Entwicklung von Leberkrebs (hepatozelluläres Karzinom, HCC). Die 5-Jahresinzidenz sank beispielsweise in einer Studie von 13,7 % (Placebogruppe) auf 3,7% in der Entecavir-Gruppe. 18 19
HBV-Infektion bei Immuntoleranz
Patienten mit HBV-Infektion aber normalen Transaminasen sind wahrscheinlich weitgehend immuntolerant und zeigen keine oder nur eine geringe Fibrosebildung. Das Zirrhoserisiko wird als so gering eingeschätzt, dass eine antivirale Behandlung nicht empfohlen wird. 20 21 Solch eine Immuntoleranz zeigen Neugeborene mit einer vertikalen HBV-Transmission von der infizierten Mutter. In der ersten Phase ist die Virusreplikation sehr hoch, das HBeAg ist nachweisbar und die Transaminasen sind nur minimal erhöht. Auch bei jungen Menschen unter 30 Jahren findet sich häufig solch eine Anfangsphase.
Wird das Immunsystem medikamentös unterdrückt, beispielsweise durch Rituximab, so ist bei „schlafender“ HBV-Infektion eine Reaktivierung zu gewärtigen, die zu einem fulminanten Leberversagen führen kann. 22
Koinfektionen
HBV-HCV-Koinfektion
Das HCV hemmt die Replikation des HBV bei einer Koinfektion. Wird HCV durch neuere antivirale Medikamente (Direct-acting agents, DAAs) unterdrückt, kann es zu einer Reaktivierung einer HBV-Erkrankung kommen. Es wird angenommen, dass besondere virale Mutationen mit solch einer Reaktivierung zu tun haben. Um die Entwicklung einer chronischen HBV-Infektion zu verhindern, ist dann eine antivirale Therapie gegen Hepatitis B indiziert, die evtl. zuvor nicht erforderlich war. 23
HBV-HIV-Koinfektion
Sie ist individuell zu gestalten. Als Die Standardbehandlung wird pegyliertes Interferon alfa-2a (Pegasys) oder -2b (Peg-Intron) plus Ribavirin für 48 Wochen empfohlen. Darunter soll eine Ansprechrate von 14 % bis 29 % bei Genotyp 1 und 53 % bis 73 % bei Genotyp 2 und 3 erwartbar sein. 24
Neue Entwicklungen
Die Behandlung der chronischen HBV-Infektion ist durch hohe Neigung zu Relapsen (Wiederauftreten) problematisch. Die Methoden einer Gentherapie eröffnen neue Optionen. Sie umfassen (nach 9 ):
- die Gen-Stummschaltung durch Nutzung der RNA-Interferenz,
- die Transkriptionshemmung durch epigenetische Modifikation der Ziel-DNA,
- die Veränderung des Genoms durch Designernucleasen und
- die Immunmodulation mit Cytokinen.
Ergebnisse von Studien hierzu müssen abgewartet werden.
Weitere Hoffnungen liegen auf der Entwicklung von neuen Medikamenten, 25
- die den Eintritt von HBV in Leberzellen (Hepatozyten) blockieren,
- die den cccDNA-Pool erschöpfen,
- die die Kernassemblierung beeinflussen,
- die RNase-H abbauen.
Gleichzeitig sollten die Immuntherapie und neue Impfstoffe Fortschritte ermöglichen. 26
Eine chronische HBV- oder HCV-Infektion wird nicht als Kontraindikation für eine Therapie mit Checkpoint-Inhibitoren angesehen, wenn diese im Rahmen einer Krebstherapie erforderlich sind. 27
Xalnesiran ist ein kleines RNA-Molekül, das die Vermehrung des Hepatitis-B-Virus hemmt. Eine Phase-II-Studie an Patienten mit einer chronischen Hepatitis B unter Therapie mit Entecavir oder Tenofovir bewirkte Xalnesiran (zusammen mit PEG-Interferon alpha-2a) innerhalb 24 Wochen in 23 % eine Abnahme der Viruslast unter die Nachweisgrenze von 1000 IE pro Milliliter und eine Serokonversion (Nachweis der Abwehrreaktion im Patientenblut) in 20 % der Fälle. In 50 % kam es zu unerwünschten Ereignissen (meistens eine Erhöhung von Transaminasen). 28
Impfung
Es ist das Ziel der WHO, HBV bis 2030 über Impfkampagnen weltweit zu eliminieren. 29
Die Impfung gegen Hepatitis B hat eine Immunisierung zum Ziel, die bewirkt, dass die Wahrscheinlichkeit für den Ausbruch einer Hepatitis nach Infektion mit HBV stark gesenkt wird. Die Schutzwirkung hängt vom erzielten Antikörpertiter ab.
→ Auf facebook informieren wir Sie über Neues und Interessantes!
→ Verwalten Sie Ihre Laborwerte mit der Labor-App Blutwerte PRO – mit Lexikonfunktion.
Verweise
- Hepatitis-Serologie
- Hepatitis B Diagnostik
- Hepatitis-B-Impfung und Prophylaxe
- Hepatitis B-Chronizität bei Neugeborenen
- Vorbeugende Maßnahmen
- Hepatitis D
- HBV-HIV-Koinfektion
- Hepatitis
- chronische Hepatitis
- Leberzirrhose
- Hepatitis B – einfach erklärt
- Hepatitis B-Leitlinie AWMF
Weiteres
- Clin Microbiol Rev. 2020 Feb 26;33(2):e00046-19. DOI: 10.1128/CMR.00046-19. PMID: 32102898; PMCID: PMC7048015.[↩]
- World J Gastroenterol. 2016 Oct 21;22(39):8720-8734[↩]
- Am J Obstet Gynecol. 2016 Jan;214(1):6-14. DOI: 10.1016/j.ajog.2015.09.100. Epub 2015 Oct 8. PMID: 26454123.[↩]
- Clin Infect Dis. 2021 Nov 2;73(9):e3324-e3332. doi: 10.1093/cid/ciaa1939. PMID: 33395488.[↩]
- Clin Liver Dis (Hoboken). 2024 Apr 26;23(1):e0134. doi: 10.1097/CLD.0000000000000134[↩]
- J Gastroenterol Hepatol. 2002 Apr;17(4):409-14[↩]
- J Infect Dis. 2017 Nov 16;216(suppl_8):S771-S777. doi: 10.1093/infdis/jix355.[↩]
- Gastroenterol Clin North Am. 2020 Jun;49(2):215-238. DOI: 10.1016/j.gtc.2020.01.003[↩][↩]
- Genes (Basel). 2018 Apr 12;9(4). pii: E207. doi: 10.3390/genes9040207.[↩][↩]
- Am J Gastroenterol. 2005 Nov;100(11):2463-71[↩]
- GUT 2003; 52: 420-424[↩]
- N Engl J Med. 2003 Feb 27;348(9):808-16[↩]
- Expert Opin Biol Ther. 2007 May;7(5):751-61[↩]
- Ann Intern Med. 2007 Dec 4;147(11):745-54. doi: 10.7326/0003-4819-147-11-200712040-00183. Epub 2007 Oct 1. PMID: 17909201.[↩]
- Pharmacotherapy. 2006 Dec;26(12):1745-57[↩]
- World J Gastroenterol. 2010 Nov 21;16(43):5447-51[↩]
- Med Sci Monit. 2017 Nov 2;23:5230-5236. DOI: 10.12659/msm.903382 . PMID: 29095799; PMCID: PMC5680675.[↩]
- Hepatology. 2013 Jul; 58(1):98-107.[↩]
- Antivir Chem Chemother. 2020 Jan-Dec;28:2040206620921331. DOI: 10.1177/2040206620921331. PMID: 32418480; PMCID: PMC7232045.[↩]
- Z Gastroenterol 2004; 42: 677-8[↩]
- J Hepatol 2003; 39: 3-25[↩]
- Semin Hematol. 2010 Apr;47(2):187-98. DOI: 10.1053/j.seminhematol.2010.01.002. PMID: 20350666.[↩]
- Rev Med Virol. 2018 Jul;28(4):e1984. DOI: 10.1002/rmv.1984. Epub 2018 May 15. PMID: 29761585; PMCID: PMC6233878.[↩]
- Trop Gastroenterol. 2008 Jul-Sep;29(3):136-47. PMID: 19115605.[↩]
- JN Engl J Med. 2023 Jan 5;388(1):55-69. doi: 10.1056/NEJMra2211764.[↩]
- J Clin Med. 2020 Oct; 9(10): 3187. Published online 2020 Oct 1. doi: 10.3390/jcm9103187[↩]
- J Immunother Precis Oncol. 2024 May 2;7(2):111-121. doi: 10.36401/JIPO-23-28[↩]
- N Engl J Med 2024;391:2098-2109, DOI: 10.1056/NEJMoa2405485[↩]
- Clin Microbiol Rev. 2020 Feb 26;33(2):e00046-19. DOI: 10.1128/CMR.00046-19.[↩]
