Das Wichtigste
Cholangiokarzinom (cholangiozelluläres Karzinom, cholangioläres Karzinom, abgekürzt CCA, oft auch CCC) bedeutet Krebs der Gallenwege. Es tritt in verschiedenen Formen auf. Häufig wird es erst sehr spät diagnostiziert, sodass eine Heilung nicht mehr infrage kommt. Es gibt neue Therapieoptionen. Je nach Lokalisation werden verschiedene Typen unterschieden. Sie haben unterschiedliche Konsequenzen für die Therapie.
Diagnostik: Die Krankheit bleibt oft lange Zeit klinisch stumm. Daher wird die Diagnose selten rechtzeitig genug gestellt, dass eine Heilung noch möglich ist. Erste Symptome können gelbe Augen (Sklerenikterus), dunkler Urin, heller werdender Stuhl und ggf. Unwohlsein im mittleren und rechten Oberbauch sein. Bestätigt wird die Diagnose durch bildgebende Verfahren (Sonographie, CT, MRCP) und durch eine Gewebeprobe (Histologie). Die Bildgebung unterschätzt die tatsächliche Ausbreitung häufig.
Bahandlung: Die Behandlung ist in den meisten Fällen palliativ. Neuere Biologika, haben einen Fortschritt im Überleben gebracht. In seltenen Fällen kann eine Lebertransplantation eine Heilung bewirken. Eine Leberteilresektion mit heilender Absicht (R0-Resektion) erbringt eine deutliche Lebensverlängerung.
Typen und Entstehung
Wegen unterschiedlicher Herkunft, Therapieoptionen und Prognose werden verschiedene Typen des Gallengangskarzinoms differenziert.
Häufigkeit
Intrahepatische periphere Cholangiokarzinome stellen 5 – 10 % der primären malignen Lebertumoren dar. Männer sind häufiger betroffen als Frauen. Das Durchschnittsalter liegt bei 55 Jahren. Bei 20 % besteht gleichzeitig eine Leberzirrhose, bei 60 % eine Cholelithiasis.
Prädisposition
Das Risiko für ein Cholangiokarzinom ist bei folgenden Erkrankungen erhöht 1:
- Gallensteine (Cholelithiasis), speziell Hepatolithiasis,
- Caroli-Syndrom,
- Leberparasiten (insbesondere Clonorchis sinensis),
- Primäre sklerosierende Cholangitis (PSC),
- Dauerausscheider von Salmonella typhimurium (möglicherweise),
- Chronische Hepatitis B und chronische Hepatitis C. 2
Exogen-toxische Ursachen sind nicht bekannt.
Pathologie
Makroskopisch ist das Cholangiokarzinom der intrahepatischen Gallenwege ein weißlich markiger Tumor. Histologisch handelt es sich um einen muzinbildendes Adenokarzinom. Der Differenzierungsgrad reicht von hoch über mäßig bis zu gering differenziert (Grad 1 bis Grad 3).
Symptomatik
Das intrahepatische Cholangiokarzinom ist lange Zeit klinisch stumm. Eine lokale Einengung und ein kompletter Verschluss kleinerer intrahepatischer Gallengangsäste durch den Tumor kann zu einer lokalen Cholangitis führen, die zu unbestimmtem Druckgefühl im rechten und mittleren Oberbauch beitragen kann. Im fortgeschrittenen Stadium führt eine Verengung oder ein Verschluss des Gallengangs zu einer obstruktiven Cholestase mit Ikterus und Juckreiz. Hinzu kommen Abgeschlagenheit, Übelkeit, Inappetenz und Gewichtsverlust bis hin zur Tumorkachexie.
Diagnostik
Sonographie
Die Sonographie ist meistens die erste bildgebende Diagnostik. Sie zeigt den Tumor, die gestauten proximalen und die nicht gestauten distalen Gallenwege (siehe hier). Beim intrahepatischen Cholangiokarzinom kann der Tumor überall im Lebergewebe gefunden werden. Oft veranlasst er eine langwierige und erfolglose Primärtumorsuche, bis schließlich eine (z. B. Sonographie- oder CT-gestützte) Punktion des Leberherdes und die histologische Untersuchung des Punktionszylinders die Diagnose ergibt.
Eine Lokalisation des Leberherds in der Leberpforte lässt an einen Klatskin-Tumor denken. Die Gallenblase ist dabei unauffällig und wegen der Abflussstöung aus der Leber nur sehr gering gefüllt.
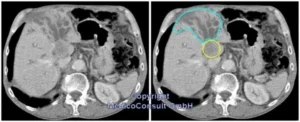
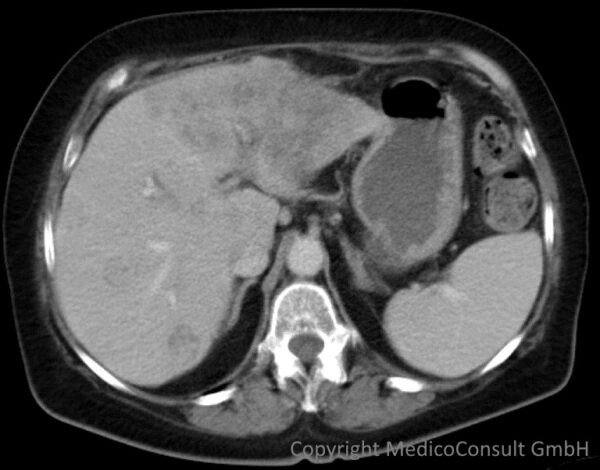
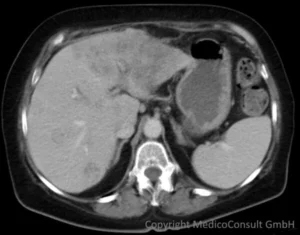
CT
Die Computertomographie (CT) hat einen ähnlichen Aussagewert und ergänzt die Sonographie.
MRT / MRCP
Die Magnetresonanztomographie (MRT) vermag zusammen mit der MR-Cholangiographie (MRCP) wichtige präoperative Informationen (Lokalisation, Stenosierung, Infiltration, Gefäßbeteiligung) zu geben. Zwischen den Befunden bildgebender Verfahren und dem operativen Befund bestehen manchmal Diskrepanzen, die auf einer mikroskopischen Ausbreitung des Tumors (entlang der Mukosa und in den Perineuralscheiden) beruht. Eine solche Ausbreitung kann makroskopisch und in der Bildgebung nicht erkennbar sein. 3
ERC
Die ERC (endoskopische retrograde Cholangiographie) ist die beste Methode, wenn es darum geht, ein Hindernis im Gallenwegsystem zu erkennen und zu lokalisieren und in diesem Fall auch gleich eine Galleableitung zu etablieren. Wenn es nur darum geht, eine Diagnostik und nicht auch gleich eine Therapie durchzuführen, reicht eine MRCP, die das invasive Risiko nicht trägt. Eine ERC ermöglicht dagegen nicht nur eine Darstellung der Tumorobstruktion, sondern meist auch die Gewinnung einer Gewebeprobe und / oder einer Galleprobe (z. B. für eine bakteriologische Untersuchung). Und sie kann in geeigneten Fällen zur Einlage eines Stents an der Tumorverengung vorbei zum Zweck einer Galledrainage genutzt werden.
Cholangioskopie
Die Cholangioskopie ist eine Methode zur direkten Besichtigung der größeren Gallengänge mit Hilfe eines dünnen Endoskops. Wenn der Gallengangstumor durch das Endoskop erreichbar ist, kann eine gezielte Biopsie für eine histologische Untersuchung entnommen werden.
Gewebeprobe (Punktion)
Die Entnahme einer Gewebeprobe sollte nur bei geplanter palliativer Therapie entnommen werden. Eine routinemäßige Entnahme einer Gewebeprobe vor einer kurativ geplanten Operation wird wegen möglicher Zellverschleppung möglichst vermieden!
Laborwerte
Da das Gallenwegskarzinom i.d.R. durch Ikterus und entfärbten Stuhl auffällt, sind meist die Cholestaseparameter (Bilirubin, alkalische Phosphatase, Gamma-GT) erhöht. Sie sinken nach Drainage der gestauten Gallenwege.
Bei einer sekundär entstandenen Cholangitis sind die Entzündungsparameter und die Leukozytenzahl im Blut erhöht.
Als Verlaufsparameter der Krebsausbreitung kann in den meisten Fällen der Tumormarker CA 19-9 dienen.
Differenzialdiagnosen
Differenzialdiagnosen des intrahepatischen Cholangiokarzinoms
Das intrahepatische Cholangiokarzinom wird histologisch diagnostiziert und von anderen Leberherden abgegrenzt.
- Hepatozelluläres Karzinom (HCC). In Zweifelsfällen kann eine Cytokeratinfärbung den Tumor vom hepatozellulären Karzinom differenzieren.
- FNH (bei Frauen)
- Leberadenom
- Metastasen von intestinalen Adenokarzinomen. Eine positive Färbung mit Anticytokeratin 20 spricht gegen ein Gallengangskarzinom und eher für eine Metastase.
Differenzialdiagnosen des extrahepatischen
Der Klatskin-Tumor der Leberpforte kann zu folgenden differenzialdiagnostischen Überlegungen führen:
- Gallenblasenkarzinom mit Einbruch in die Leberpforte,
- zentraler Tumor anderer Genese (HCC, Lebermetastase, Echinokokkuszyste),
- Striktur bei primärer sklerosierender Cholangitis).
→ Zum Klatskin-Tumor siehe hier.
Therapie
Interventionelle Therapie
Lebertransplantation: In seltenen Fällen kann sie mit Aussicht auf Heilung infrage kommen 4
Eine Operation kann bei günstiger Größe und Lage des Karzinoms in Frage kommen. Die Erfolgsrate ist jedoch gering. In einer Zusammenstellung wurden das mediane Gesamtüberleben und das krankheitsfreie Überleben mit 1,66 bzw. 0,79 Jahren angegeben. 5 Eine andere Zusammenstellung berichtet von einem 5-Jahresüberleben nach R0-Resektion (also nach kurativer Operation ohne erkennbaren Resttumor) von 20%-42%. 6
Lebertransplantation bei inoperablem hCCA oder bei hCCA im Rahmen einer PSC: Wenn der Tumor kleiner als 3 cm ist und kein Anzeichen von Metastasen vorliegen, kann eine neoadjuvante Radiochemotherapie mit anschließender Lebertransplantation zu einer deutlichen Lebensverlängerung führen. Die 5-Jahres-Überlebensrate liegt bei etwa 60 %. 7.
Leberresektion und Lebertransplantation bei iCCA: Beim iCCA kommt in ausgewählten Fällen eine ausgedehnte Leberresektion (LR) infrage. Pflicht ist eine Lymphadenektomie von mindestens 6 Lymphknoten. Bei mehr als 40 % der Patienten wurden mikroskopische Lymphknotenmetastasen nachgewiesen. Die 5-Jahres-Gesamtüberlebensrate liegt zwischen 25 % und 40 %. Eine Lebertransplantation (LT) wird als eine Behandlungsoption für Patienten mit inoperablem iCCA im sehr frühen Stadium (d. h. ≤ 2 cm) angesehen. Studien fehlen 8.
Gallenwegsdrainage: Eine endoskopische Intervention (ERCP) ist bei zentraler Einengung der Gallenwege dann indiziert, wenn eine Drainage der gestauten Gallenwege durch Stenteinlage angestrebt wird. Eine Drainage kann auch perkutan transhepatisch erfolgen (PTD, perkutane transhepatische Drainage). Sie kann bei inoperablen Fällen eine Verbesserung der Symptomatik (Ikterus, Juckreiz, Verdauungsstörungen) bewirken.
Gallenwegsdrainage vor geplanter Leberteilresektion: Eine biliäre Drainage mit Einführung eines Katheters oder Stents führt zu einer deutlichen Abnahme der Genauigkeit der Ausbreitungsdiagnostik, so dass sie bei geplanter Teilresektion erst nach Abschluss des Stagings erfolgen sollte, und auch nur dann, wenn zweizeitig behandelt werden soll. 9 Die chirurgischen Verfahren erfordern die Resektion eines großen Teils auch des gesunden Leberparenchyms (Sicherheitsabstand), so dass oft zunächst eine Vergrößerung der verbleibenden Restleber zur Vermeidung einer postoperativen Leberinsuffizienz erforderlich werden kann. In diesen Fällen ist eine Gallenwegsdrainage eine sinnvolle Zwischenmaßnahme. Ansonsten wird ein einzeitiges Vorgehen vorgezogen und auf eine präoperative Drainage verzichtet. 6
Chemotherapie und Strahlentherapie
Chemotherapie: Das intrahepatische Cholangiokarzinom spricht schlecht auf Chemotherapie an. Regime, die ein Ansprechen erwarten lassen, beinhalten 5-Fluorouracil, Doxorubicin, Adriamycin und cis-Platin. Häufig wird die Kombination Gemcitabin plus Cisplatin (GC) angewendet. 10 Die Kombination mit Durvalumab, einem Anti-PD-1-Antikörper, bringt weitere Überlebensvorteile (s. u.).
Radiochemotherapie: Die Regime werden häufig im Rahmen einer multimodalen Therapie zusammen mit einer Strahlentherapie angewandt. In einer Studie wurde eine Remissionsrate von 33,3 % berichtet; die Patienten, die ansprachen, hatten ein mittleres Überleben von 15,2 Monaten 11.
Durch Bestrahlung oder Chemotherapieregime (FAM, EMFL) ist bisher keine entscheidende Lebensverlängerung erzielt worden. Eine Sondersituation besteht beim Klatskin-Tumor. In Einzelfällen kann Gemcitabin bzw. eine Gemcitabin-basierte Chemotherapie zur Lebensverlängerung beitragen. 12 13 Dabei kann mit einer Ansprechrate bis zu 30% und ein mittleres Überleben von ca. 15 Monaten gerechnet werden.
Hochenergetische Strahlen können von außen mit Hilfe von „CyberKnife (TM)“ stereotaktisch sehr gezielt appliziert werden. In einer Studie an 34 Patienten mit intrahepatischen und hilären Chonangiokarzinomen lag die mittlere progressionfreie Zeit unter dieser Therapie bei 10 Monaten und die mittlere Überlebenszeit bei 17 Monaten 14.
Eine Gegenüberstellung einer Radiochemotherapie (RCT) und einer reinen Chemotherapie an einer großen Fallzahl (n=2842) ergab einen leichten Vorteil für die RCT (Überlebenszeit 13,6 vs. 10,5 Monate). 15
Immun-Checkpoint-Inhibitoren
Immun-Checkpoint-Inhibitoren (ICIs) zeigen einen gewissen lebensverängernden Effekt. 16 Der Anti-PD-L1-Hemmer Durvalumab scheint eine neue Option darstellen zu können. 17 Insbesondere Mittel, die gegen den Fibroblasten-Wachstumsfaktor gerichtet sind, wie Pemigatinib, scheinen aussichtsreich zu sein. Die Isocitratedehydrogenase 1 (IDH1) scheint in bestimmten Fällen ebenfalls ein aussichtsreiches Ziel zu sein. 18 19 20
Wird eine hohe Mikrosatelliten-Instabilität (MSI) gefunden, so kann der PD-1-Hemmer Pembrolizumab (ein Apoptosehemmer) laut Einzelbeobachtungen die Lebenszeit deutlich verlängern, auch wenn eine Chemotherapie zuvor erfolglos war. (Eine MSI zeigt eine defekte DNA-Reparaturfunktion im Zellkern an; es sammeln sich fehlerhafte Kopien.) Vor einer Therapie mit diesem Hemmer des programmierten Zelltods wäre entsprechend die Testung auf Mikrosatelliteninstabilität zu empfehlen. 21 22
Eine real-world-Studie mit einem PD-1-Hemmer (verwendet wurden Nivolumab, Pembrolizumab, Toripalimab, Camrelizumab, Sintilimab oder Tislelizumab) an chinesischen Patienten mit fortgeschrittenem iCCA erbrachte eine mittlere Gesamtüberlebenszeit und progressionsfreie Überlebenszeit von 19,3 Monaten und 11,6 Monaten. 23
FGFR-Hemmer: Pemigatinib (ein selektiver oraler Inhibitor von FGFR1, 2 und 3) erbrachte bei fortgeschrittenem CCC ein mittleres progressionsfreies Überleben von 6,9 Monaten und ein Gesamtüberleben von 21 Monaten. 24 Der Pan-FGFR-Hemmer ist auch bei anderen Tumoren wirksam, insbesondere bei Nachweis von FGFR-Fusionen oder -Umlagerungen oder FGFR-Mutationen. 25 Erklärung: FGFR (fibroblast growth factor receptor) ist eine Familie von 4 Rezeptoren mit assoziierter Tyrosinkinase, die bei der Embryogenese und Organogenese eine biologische Rolle spielen. Bei geschätzt 15–20 % der Fälle von intrahepatischem Cholangiokarzinom (iCCA) finden sich FGFR2-Veränderungen. 26
Kombinationen: Einzelbeobachtungen besagen, dass bestimmte Kombinationen von Biologika zu einer Verlängerung des Überlebens beim iCCA führen können. Beispiel: In einem Fall von metastasiertem iCCA, bei dem die Erstlinientherapie mit einem PD-1-Inhibitor in Kombination mit einem Tyrosinkinase-Inhibitor (TKI) versagt hatte, wurde eine Zweitlinienbehandlung mit Lenvatinib (ein Tyrosinkinase-Inhibitor) in Kombination mit Trifluridin/Tipiracil (TAS-102) begonnen. Die Behandlung führte zu einer signifikanten Tumorschrumpfung ohne dass Nebenwirkungen des Grades 3 oder höher auftraten. Das progressionsfreie Überleben (PFS) betrug 13,33 Monate 27.
Durvalumab, ein gegen den programmierten Zelltod-Liganden 1 (PD-L1) gerichteter Antikörper, hat in Kombination mit Gemcitabin und Cisplatin die Zulassung der FDA für die Behandlung von fortgeschrittenem Gallengangskarzinom erhalten. Die Überlebensrate betrug nach 2 Jahren 23,6 % in der Durvalumab-Gemcitabin-Cisplatin-Gruppe und 11,5 % in der Gruppe, die mit Placebo plus Gemcitabin-Cisplatin behandelt wurde 28.
→ Signalwege und Checkpoints: Basics
→ facebook: Neues und Interessantes!
→ Labor-App Blutwerte PRO – mit Lexikonfunktion
Verweise
Weiteres
- Eur Rev Med Pharmacol Sci. 2010 Apr;14(4):363-7[↩]
- BMC Cancer. 2012 Jul 16;12:289. doi: 10.1186/1471-2407-12-289[↩]
- Manfredi R et al. Semin Liver Dis 2004; 24: 155-164[↩]
- Lancet. 2014 Jun 21;383(9935):2168-79. DOI: 10.1016/S0140-6736(13)61903-0[↩]
- World J Hepatol. 2020 Sep 27;12(9):641-660. doi: 10.4254/wjh.v12.i9.641. PMID: 33033570; PMCID: PMC7522563.[↩]
- World J Gastroenterol. 2020 Jul 7;26(25):3542-3561. DOI: 10.3748/wjg.v26.i25.3542[↩][↩]
- Surg Clin North Am. 2024 Feb;104(1):183-196. doi: 10.1016/j.suc.2023.09.004[↩]
- J Hepatol. 2020 Feb;72(2):364-377. doi: 10.1016/j.jhep.2019.11.020.[↩]
- World J Surg. 2018;42:3676–3684. DOI: 10.1007/s00268-018-4654-2[↩]
- Ann. Oncol. 2016;27:v28–v37. doi: 10.1093/annonc/mdw324[↩]
- Int J Radiat Oncol Biol Phys. 1987 May;13(5):687-95[↩]
- World J Gastroenterol. 2008 Nov 28;14(44):6876-80[↩]
- Expert Opin Pharmacother. 2005 Feb;6(2):211-23[↩]
- J Cancer. 2015 Aug 1;6(11):1099-104[↩]
- J Gastrointest Oncol. 2018 Jun;9(3):527-535. doi: 10.21037/jgo.2018.01.15.[↩]
- Cancers (Basel). 2022 Mar 29;14(7):1748. DOI: 10.3390/cancers14071748[↩]
- Drugs. 2021 Apr;30(4):343-350. doi: 10.1080/13543784.2021.1897102[↩]
- Medicina (Kaunas). 2021 May 8;57(5):458. DOI: 10.3390/medicina57050458[↩]
- Lancet Oncol. 2020 May;21(5):671-684. DOI: 10.1016/S1470-2045(20)30109-1.[↩]
- Life (Basel). 2023 Oct 16;13(10):2066. doi: 10.3390/life13102066[↩]
- JGH Open. 2021 May 21;5(6):712-716. DOI: 10.1002/jgh3.12576[↩]
- Clin J Gastroenterol. 2021 Jun 3. DOI: 10.1007/s12328-021-01458-8[↩]
- Ann Med. 2022 Dec;54(1):803-811. DOI: 10.1080/07853890.2022.2048416.[↩]
- Lancet Oncol. 2020 May;21(5):671-684. DOI: 10.1016/S1470-2045(20)30109-1[↩]
- Ann Oncol. 2022 May;33(5):522-533. DOI: 10.1016/j.annonc.2022.02.001.[↩]
- Cancer Discov. 2021;11:326–339. doi: 10.1158/2159-8290.CD-20-0766[↩]
- Front Oncol. 2025 Dec 4;15:1695911. doi: 10.3389/fonc.2025.1695911[↩]
- Lancet Gastroenterol Hepatol. 2024 Aug;9(8):694-704. doi: 10.1016/S2468-1253(24)00095-5[↩]