Das Wichtigste verständlich
| Die Porphyrie ist eine genetisch bedingte Stoffwechselkrankheit, bei der in unterschiedlicher Zusammensetzung und Stärke Blasen und Geschwüre (Ulzerationen) an lichexponierten Stellen, Bauchschmerzen und Krämpfe sowie neurologische und psychiatrische Symptome verschiedener Art auftreten. Es werden eine Reihe von Untergruppen unterschieden. Gemeinsam ist ihnen eine Störung der Häm-Biosynthese, die unter der Wirkung auslösender Faktoren zu lebensbedrohlichen Stoffwechselkrisen führen kann.
Entstehung: An unterschiedlichen Stellen des Häm-Stoffwechsels fehlen funktionstüchtige Enzyme. Häm kommt in verschiedenen biologischen Molekülen, wie Hämoglobin (roter Blutfarbstoff, zuständig für den Sauerstofftransport im Blut) und Cytochromen (komplexe Enzyme in Mitochondrien, die für die Energiegewinnung und den Endabbau von Stoffwechselprodukten zuständig sind) vor. Es ist diejenige chemische Gruppe, die Sauerstoff zu binden vermag. Je nachdem, an welcher Stelle die Bildung des Häm gestört ist, kommt es zu unterschiedlichen Formen der Porphyrie.
ANZEIGE
Formen: Die Porphyrien werden in erythropoetische und hepatische Formen unterschieden. Die häufigste Form ist die Porphyria cutanea tarda (PCT). Symptome: Zu den schwerwiegendsten Symptomen einer Porphyrie gehören
Auslösung: Die Symptomatik kann durch besondere Lebensumstände, Alkohol und eine Reihe von Medikamenten ausgelöst werden. Ein Auslöser kann eine lebensbedrohliche Porphyriekrise hervorrufen. Diagnostik: Die Diagnostik beinhaltet einen Nachweis von Gesamtporphyrinen und der Delta-Aminolävolinsäure im Urin. Eine genaue Differenzierung der im Urin nachweisbaren Stoffwechselprodukte führt zu dem jeweils vorliegenden Porphyrietyp. Eine genetische Testung naher Angehöriger vermag eine Veranlagung nachzuweisen, was für die Vorbeugung einer Porphyriekrise bedeutsam ist. Behandlung: Eine krisenhafte Verschlimmerung ist als Notfall in einer Klinik zu behandeln. Die Behandlung stützt sich auf Kohlenhydratinfusionen bei milden Attacken und Hämatin bei schweren Attacken. Die Auslöser sind zu vermeiden. 1 2 3 |
Entwicklung
Die Porphyrien entstehen durch eine Ansammlung von Stoffwechselprodukten der Porphyrine im Körper. Die meisten Formen sind genetisch bedingt.
Porphyrine sind Vorstufen in der Häm-Biosynthese. Häm bildet den Eisen-bindenden Bestandteil des roten Blutfarbstoffs (Hämoglobin); es wird auch für die Bildung von Cytochromen benötigt (Cytochrom-P450-System), die beispielsweise bei Entgiftungsprozessen in der Leber eine entscheidende Rolle spielen.
Delta-Aminolävolinsäure
Ausgangspunkt der Hämbiosynthese ist die Delta-Aminolävolinsäure (5-ALA, d-ALA), die durch die Wirkung der Delta-Aminolävolinsäure-Synthase entsteht. Die Wirkung dieses Enzyms wird durch seine Stoffwechselprodukte inklusive dem Häm durch negative Rückkopplung gehemmt. Dies kann bei der Behandlung der Porphyrie therapeutisch ausgenutzt werden (Hämarginat-Infusionen, s.u.). 4
5-ALA wird bei vielen Formen der Porphyrie akkumuliert und gilt daher als wichtiger Indikator für die Erkrankung. Sie gilt heute auch als Ursache der Schmerzen bei den akuten hepatischen Porphyrien. 5 Ihre Konzentration im Blut sowie ihre Ausscheidung mit dem Urin ist erhöht bei
- der akuten intermittierenden Porphyrie (AIP),
- der hereditären Tyrosinämie und
- der Bleivergiftung.
5-ALA bewirkt multiple Zellschädigungen durch oxidativen Stress mit Schädigung von Eiweißkörpern, Zellstrukturen und DNA. Sie kann apoptotische Zellschädigungen auslösen und ist karzinogen.
Emzymdefekte
Die verschiedenen Porphyrieformen unterscheiden sich durch den Schritt im Stoffwechsel auf dem Weg von der Delta-Aminolävolinsäure zum Häm, an dem die Synthese gestört ist.
- Die ALAD-Porphyrie (Doss-Porphyrie, eine extrem seltene Porphyrieform 6 ) beispielsweise beruht auf einem Defekt der mitochondrialen Porphobilinogensynthase (oder ALA-Dehydratase, delta-Aminolevulinat-Dehydratase), dem zweiten Schritt der Hämbiosynthese,
- die akute intermittierende Porphyrie (AIP) weist die Störung bei der Porphobilinogen-Desaminase auf, dem dritten Schritt der Hämbiosynthese,
- die Porphyria cutanea tarda (chronische hepatische Porphyrie) bei der Uroporphyrinogen-Decarboxylase,
- die Porphyria variegata bei der Protoporphyrinogen-Oxidase,
- die kongenitale erythropoetische Porphyrie bei der Häm-Synthase,
- die Porphyria variegata bei der Protoporphyrinogenoxidase (vorletzter Schritt der Hämsynthese) und
- die erythropoetische Protoporphyrie bei der Ferrochelatase.
Die Ursache der abdominellen Schmerzen bei der akuten intermittierenden Porphyrie ist möglicherweise eine viszerale Ischämie. 7
Die Ursache neuropathischer Dysfunktionen scheint eine toxische Wirkung der 5-ALA auf den GABA-Rezeptor und eine Häm-Depletion der Nervenzellen zu sein. 8
Auslösende Faktoren
Porphyrie-Attacken mit neurovegetativen Symptomen und Bauchschmerzen sind lebensgefährlich. Sie werden durch eine Reihe von Faktoren ausgelöst:
- hormonelle Veränderungen (z.B. prämenstruell, Schwangerschaft, Antikonzeptiva)
- Alkoholkonsum
- psychischer oder physischer Stress (auch Infektionen oder Operationen)
- Arzneimittel: sie sind die wichtigsten auslösenden Faktoren (siehe hier).
Klassifikation der Porphyrien
Die Porphyrien werden grob eingeteilt in erythropoetische und hepatische Porphyrien. Die Unterscheidung berücksichtigt, dass die Geschwindigkeit der Synthese der Porphyrine unterschiedliche Engpässe aufweist: im Knochenmark ist es das Eisen und in der Leber das Häm.
Die meisten Porphyrien sind genetisch bedingt und werden autosomal dominant vererbt, so die akute intermittierende Porphyrie, die hereditäre Coproporphyrie und die Porphyria variegata (s. u.)
Erythropoetische Porphyrieformen
- Kongenitale erythropoetische Porphyrie (CEP, Morbus Günther),
- Erythropoetische Protoporphyrie (EPP),
- X-chromosomale Protoporphyrie.
Hepatische Porphyrieformen
- Akute intermittierende Porphyrie (AIP),
- Hereditäre Koproporphyrie (HCP),
- Porphyria variegata (PV),
- Porphyria cutanea tarda (PCT),
- Porphobilinogensynthase-Defizienz.
Akute Porphyrien
Akute hepatische Porphyrien sind AIP, HCP und PV. Sie sind Erkrankungen einer molekularen Fehlregulation der Hämbiosynthese, bei denen sich die Symptomatik im Gegensatz zur chronischen hepatischen Porphyrie nicht durch Anreicherung von Porphyrinen nicht in der Leber erklärt.
Chronische hepatische Prophyrie
Die chronische hepatische Porphyrie wird heute als Porphyria cutanea tarda (PCT) bezeichnet. Sie ist eine Erkrankung, die durch Anreicherung von Porphyrinen in der Leber zustande kommt. 9
Sekundäre Porphyrie
- Porphyria cutanea tarda (PCT)
Symptomatik
Klinisch lassen sich die Porphyrien in solche einteilen, die akute neuroviscerale Symptome (Bauchschmerzen, neurologische und psychiatrische Symptome) hervorrufen, und solche die Hautsymptome auslösen. Die Symptome sind alle vieldeutig und weisen nicht direkt auf eine Porphyrie hin.
Leberschaden, Leberkrebs: Als Komplikation einer Porphyrie kann es zu einer Leberschädigung mit Entwicklung einer Leberzirrhose kommen; dies gilt insbesondere für die erythropoetische Porphyrie und die Porphyria cutanea tarda. In Einzelfällen führte die erythropoetische Porphyrie zur Indikation einer Lebertransplantation. 10 Das Risiko von Leberkrebs ist erhöht: in einer Auswertung von Studien 3,3% HCC, 0,3% CCC. 11
Neurologische Symptome: Sie sind vor allem assoziiert mit der akuten intermittierenden Porphyrie (AIP), der hereditären Coproporphyrie und der Porphyria variegata. Im Vordergrund stehen verschiedenartige motorische Defekte, neuropsychiatrische Auffälligkeiten und gastrointestinale Beschwerden. 12
→ Differenzialdiagnosen von Bauchschmerzen
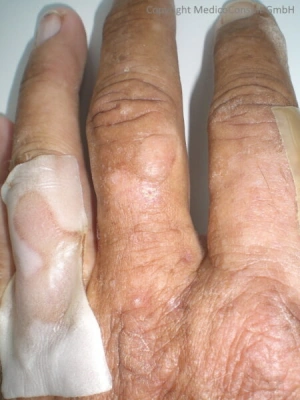
Hauterscheinungen: Die kutanen Porphyrien (insbesondere Porphyria cutanea tarda, Porphyria variegata und hereditäre Koproporphyrie) lassen sich in zwei Typen unterteilen, in diejenigen mit überwiegender Blasenbildungen und Hautbrüchigkeit und in diejenigen mit überwiegender Sonnenempfindlichkeit (Photosensitivität). 13
Differenzielle Symptomatik
Folgende Symptome kommen bei den verschiedenen Porphyrieformen vor:
- Gemeinsamkeiten akuter Porphyrien: Alle autosomal dominant vererbten akuten Porphyrien weisen ein erhöhtes Risiko für Bluthochdruck, Niereninsuffizienz und hepatozelluläres Karzinom (HCC) auf.
- Photosensitive Hautläsionen bei allen erythropoetischen und hepatischen Formen (außer bei der akuten intermittierenden Porphyrie (AIP) und der Porphobilinogensynthase-Defizienz), besonders bei der Porphyria variegata und der hereditären Koproporphyrie (narbig verheilende bullöse Hautläsionen)
- Abdominelle Schmerzattacken (z.T. äußerst heftig) treten nur bei den hepatischen Porphyrien auf.
- Hautläsionen unter Lichteinfluss finden sich bei allen Porphyrien außer der AIP.
- Neuropsychiatrische Syndrome nur bei den hepatischen Porphyrien (psychovegetative Unruhe, Sensibilitätsstörungen, motorische Polyneuropathie, Halluzinationen, Paranoia, Krämpfe)
- Roter Urin und rötliche Zähne die unter UV-Licht fluoreszieren (Erythrodontie) finden sich bei der erythropoetischen Porphyrie.
Einzelne Porphyrien
Hauptformen der Porphyrie sind unten zusammenfassend dargestellt. Ausführliche Informationen sind auf eigenen Seiten zusammengestellt.
Porphyria cutanea tarda (PCT)
Die Porphyria cutanea tarda ist die weltweit häufigste Porphyrie, jedoch im Gegensatz zu den erblichen Porphyrien ist sie eine erworbene Leberkrankheit, die möglicherweise auf dem Boden einer genetisch bedingten entsprechenden Reaktionsbereitschaft entsteht. Pathogenetisch scheint ein Abfall der Hepcidin-Produktion und damit eine erhöhte Aufnahme von Eisen in den Körper eine Rolle zu spielen. Sie führt über eine Folge von Stoffwechselschritten zu einer Erhöhung der Oxidation von Porphyrinogen zu Porphyrin. Die Therapie der Wahl besteht in Aderlässen bis zur Anämiegrenze. 14
Auslöser sind vor allem Alkohol, Hepatitis C, Rauchen und Östrogen-Therapie. Auch werden Assoziationen mit verschiedenen Chemikalien, Medikamenten (dazu gehören speziell Analgetika, Sedativa, Anästhetika, Antibiotika, Sexualhormone), Schwermetallen (bes. Blei), halogenierten Kohlenwasserstoffen, der Hämochromatose, der Leukämie, Hämoblastosen, hämolytische Anämien, einer ineffektive Erythropoese, angeborenen Bilirubintransportstörungen (Dubin-Johnson-Syndrom, Rotor-Syndrom) gefunden.
Symptome und Beschwerden der PCT
Unspezifische Symptomatik: Die Symptomatik kann sehr vielfältig sein und unterschiedliche Schweregrade erreichen. Sie reicht von unspezifischen Abdominalbeschwerden mit oder ohne Übelkeit, Erbrechen, Koliken, Obstipation und Subileussymptomatik bis hin zu akuten Schmerzkrisen mit kardiovaskulärer Dekompensation und Hyponatriämie, Depression oder einem Guillain-Barré-Syndrom mit Beinlähmung und bei Progredienz Tod durch Atemlähmung.
Assoziation der PCT mit der Hämochromatose
Die Porphyria cutanea tarda ist genetisch häufig mit der His63Asp-Mutation im HFE-Gen assoziiert, so dass bei dieser Porphyrieform häufig zu hohe Eisen- und Ferritinspiegel wie bei der Hämochromatose gefunden werden. 15 Bei der Porphyria cutanea tarda findet man überdurchschnittlich häufig die Hämochromatosegene C282Y und H63D in homo- oder heterozygoter Form. Sie sollen für die Porphyriesymptomatik prädisponieren. 16
Assoziation der PCT mit Hyponatriämie
Es werden mehrere Fälle einer Hyponatriämie bei Porphyrien berichtet, die bei zu raschem Ausgleich zur pontinen Myelinolyse (Stammhirndefekte) führen können.
Assoziation der PCT mit einer Enzephalopathie
In akuten Porphyrie-Attacken werden oft enzephalopathische und psychiatrische Veränderungen inklusive Krampfanfällen, schwerer Zunge, Depression und Halluzinationen auffällig. Die MRT-Untersuchung im akuten Anfall zeigt Veränderungen wie bei einer akuten Leukenzephalopathie, die reversibel sind. 17 18
Akute intermittierende Porphyrie (AIP)
Die akute intermittierende Porphyrie (AIP) ist die häufigste Porphyrieform. Ihre Symptomatik umfasst Schmerzen durch krampfartige Verengung der Blutgefäße im Bauchraum (vasospastische intestinale Schmerzen mit viszeralen Mangeldurchblutungen) und zusätzlich Nervenschmerzen (neuropathische Symptome), die wohl besser auf Hämarginat als auf hypertone Glukose reagieren. 19 Patienten mit AIP starben vor Einführung der Hämarginat-Therapie zu annähernd 60% während der ersten beiden Attacken! Eine neue Therapiemöglichkeit besteht in der Hemmung des überaktiven Enzyms Delta-Aminolaevulinsäuresynthase 1 (ALAS1) mit Givosiran (s. u.). 20
Selten kann die akute intermittierende Porphyrie mit hohen Transaminasen (bis > 1000 U/l) einhergehen (Intern Med 2000; 39: 45-49). Es wird von einem Fall mit pontiner Myelinolyse berichtet. 21 Im MRT kann das Bild einer posterioren Leukenzephalopathie entstehen, das offenbar reversibel sein kann. 22 Zu den zentralnervösen Symptomen gehören epileptische Anfälle und Paresen. Eine fatale Auswirkung der Porphyrie-bedingten Neuropathie kann die akute Ateminsuffizienz sein. 8
HCC-Risiko beim AIP
Die AIP geht mit einer erhöhten Inzidenz für Leberkrebs (hepatozelluläres Karzinom, HCC) einher, wofür DNA-Strangbrüche durch Stoffwechselprodukte von 5-ALA verantwortlich sein sollen. 23 Daher sollten Patienten mit einer AIP auch bezüglich einer Tumorsuche gut kontrolliert werden. Das HCC-Risiko ist auch bei der Porphyria cutanea tarda erhöht.
→ Akute intermittierende Porphyrie
Erythropoetische Protoporphyrie
Die erythropoetische Protoporphyrie ist die häufigste genetisch bedingte Porphyrie mit Entwicklung einer Lichtdermatose, im Gegensatz zu anderen Porphyrieformen typischerweise ohne Bläschenbildung, und mit erhöhtem Risiko für die Entwicklung einer cholestatischen Leberkrankheit bis hin zur Leberzirrhose und von Gallensteinen. Cholestyramin wird als aussichtsreiche Therapie in Einzelfällen beschrieben. Ansonsten kommt bei schweren Leberschäden eine Lebertransplantation in Betracht; es wird sequentiell dann auch eine Knochenmarktransplantation empfohlen.
→ Erythropoetische Protoporphyrie
Diagnostik der Porphyrien
Labor
Der Verdacht auf eine Porphyrie kann im akuten Anfall rasch durch Urinanalyse bestätigt werden. Im 24-Stundenurin (Sammlung in lichtundurchlässigem Behälter) werden Porphobilinogen (PBG), 5-Aminolevulinsäure (5-ALA, bzw. d-ALA) und Gesamtporphyrine bestimmt.
Gesamtporphyrine im Urin sind erhöht bei:
- hepatischer Porphyrie
- kongenitaler erythropoetischer Porphyrie
- akuter Bleiintoxikation
- sekundärer Koproporphyrie
Eine weitere Differenzierung erfolgt durch spezielle Methoden (z.B. HPLC).
Bei hepatischen Porphyrien außer bei der Porphyria cutanea tarda: Erhöhung der Delta-Aminolävolinsäure (5-ALA) im Urin.
Für die Diagnostik der AIP Bestimmung des erythrozytären PBG-Deaminase-Spiegels.
Für die Diagnostik der HCP Bestimmung der Porphyrine in Urin und Stuhl .
Für die Diagnostik der PV Bestimmung des Plasma-Porphyrin-Spiegels und des Fluoreszenzmusters.
HCC-Diagnostik (bei erhöhtem Risiko, s.o.): Ultraschall-Kontrollen und Bestimmung des alpha-Fetoproteins.
Bei der Porphyria cutanea tarda ist die Bestimmung der Eisenbeladung des Körpers (Ferritin, Transferrinsättigung und ggf. HFE-Gen, vgl. Hämochromatose) sinnvoll. 16
Genetische Testung
Die genetische Testung soll präsymptomatischen Patienten ermöglichen, das Risiko akuter Attacken zu minimieren. Bei den erythropoetischen Porphyrien vermag sie auch zur Familienplanung beratend herangezogen werden. Die Testmethoden weisen Erkennungsquoten von mehr als 90% für die meisten Gene aus. 24
Therapie
Bei IAP, HCP und VP werden akute Porphyrie-Attacken behandelt mit
- großen Kohlenhydatmengen (500g/d) z.B. Glukoseinfusion mit 20 g/h: sie unterdrücken wie Hämatin die Aktivität der ALA-Synthase, haben aber nur bei milden Attacken einen ausreichenden Effekt,
- Hämatin i.v. (engl. hemin); neuere Medikation: Hämarginat (Normosang®): 3 mg/kg Körpergewicht, maximal 250 mg/Tag 1x pro Tag über 4 Tage (siehe unter Informationen zu Normosang®). Hämarginat ist Therapie der Wahl bei schweren Attacken.
- Givosiran: Dies ist ein neues RNA-Interferenztherapeutikum, das die bei der IAP erhöhte Synthese des Enzyms ALAS1 in der Leber hemmt. Es verringert die Akkumulation von neurotoxischen Porphyrin-Vorläufern bei Patienten mit AHPs. In einer Studie kam es bei einer einmal monatlichen Applikation darunter fast zu einer Normalisierung der ALAS1-messenger-RNA (mRNA), der Deltaaminolevulinsäure und des Porphobilinogens. Die jährlich Rate an Attacken wurde um 79 % reduziert. 25 Die höhere Wirksamkeit war mit einer höheren Rate hepatischer und renaler Nebenwirkungen verbunden. 26 27
Substanzen, die potentiell eine Porphyrie auslösen können (u. a. Medikamente, siehe oben), müssen vermieden werden.
Vitamin E: Hohe Dosen von Vitamin E vermindern die Porphyrinausscheidung bei der Porphyria cutanea tarda. Als Ursache wird diskutiert, dass reaktive Sauerstoffspezies, die mit dem Enzym interferieren, von dem antioxidativ wirkenden Vitamin E abgefangen werden, womit die Aktivität der Uroporphyrinogendecaboxylase (UROD) gesteigert wird. 28 Dies wurde bei der Porphyria variegata bestätigt. 29
Neurolyse: In einem Fall heftigster abdomineller Schmerzen konnte eine Verbesserung durch Neurolyse des Ganglion coeliacum bewirkt werden. 30
Melatonin: Melatonin ist ein wirksames Antioxidans und vermag wahrscheinlich gegen den oxidativen Stress durch 5-ALA und auch gegen seine karzinogene Wirkung zu schützen. 31 Dies legen auch tierexperimentelle Untersuchungen nahe. 32
Eisenreduktion: Die Porphyria cutanea tarda ist assoziiert mit Eisenüberladung der Leber und profitiert von einer Eisenreduktionstherapie (ebenso wie die Hämochromatose). 33
Schmerzbehandlung
Empfehlungen Stand 2022: 34
- Zur Behandlung akuter Schmerzattacken werden Opiate in Kombination mit Hämininfusionen empfohlen.
- Chronische Schmerzen sollten mit Gabapentinoiden und bestimmten Antidepressiva (vor Opiaten) behandelt werden.
- Givosiran, das die ALA- und PBG-Spiegel senkt, hat wahrscheinlich einen langfristigen Nutzen bei chronischen Schmerzen. Es sollte früh im Krankheitsverlauf begonnen werden.
Lebertransplantation
Eine Lebertransplantation kann indiziert sein: 35
- im Endstadium einer Porphyrie-assoziierten Leberzirrhose z. B. bei der erythropoetischen Protoporphyrie. Bei dieser Porphyrieform wäre allerdings vor allem die Knochenmarktransplantation eine Therapieoption.
- bei lebensbedrohlichen Porphyrie-Schüben, insbesondere bei der akut-intermittierenden Porphyrie (AIC). Die Lebertransplantation ist in diesem Fall kurativ (heilend)!
Erlaubte und nicht erlaubte Medikamente
Akute Porphyrie-Schübe können durch Medikamente ausgelöst werden. Um ihnen vorzubeugen, sollten unsichere Medikamente unbedingt vermieden werden. Die Liste wird jeweils von der europäischen Drug Database vervollständigt und ist hier einsehbar.
Liste angeblich sicherer Medikamente
Eine Liste angeblich sicherer Medikamente wird im Internet zur Verfügung gestellt (siehe hier).
- Analgetika und NSAR
Azetaminophen, Acetylsalizylsäure, Kodein, Fentanyl, Morphin und Verwandte, Dihydrocodein, Paracetamol
- Antibiotika
Penicilline, Cephalosporine, Aminoglykoside, Tetrazyklin
- Psychoaktive Medikamente und Sedativa
Chloralhydrat, Haloperidol, Lithium, Midazolam, Nortryptilin, Oxazepam, Paraldehyd, Promazin
- Antihypertonika und Diuretika
Amilorid, Atenolol, Ethakrynsäure, Propranolol, Reserpin, Triamteren
- Andere
Aciclovir, Atropin, Cimethidin, Dicumarol, Glukokortikoide, Heparin, Insulin, Neostigmin, Pethidin, Procain, Thyroxin, Chlorpromazin
Liste angeblich unsicherer Medikamente
Nach einer Liste im Internet (siehe hier):
- Analgetika und NSAR
alle NSAR außer ASS, Phenacetin, Phenylbutazon, Tilidin, Pentazocin, Tramadol, verschiedene Antibiotika,
- Antimykotika
Chloramphenicol, Doxycyclin, Metronidazol, Sulfonamide, Griseofulvin
- Herz-Kreislaufmittel
Amiodaron, Nifedipin, Verapamil
- Psychoaktive Medikamente und Sedativa
Barbiturate, Diazepam, Meprobamat
- Antihypertonica und Diuretika
Alpha-Methyldopa, Captopril, Clonidin, Furosemid, Hydralazin, Spironolacton, Thiazide
- Andere
Ergotaminpräparate, Imipramin, Östrogene, Sulfonylharnstoffe, Theophyllin, Tolbutamid, Metamizol, zunächst allgemein alle neu zugelassene Medikamente
Behandlung besonderer Symptome
Wenn Patienten mit Porphyrie wegen anderweitiger Symptome behandelt werden sollen, können – unter besonderer Berücksichtigung der Liste angeblich sicherer und unsicherer Medikamente – wahrscheinlich folgende Medikamente bzw. Medikamentengruppen verwendet werden:
- Tachykardie: ggf. ß-Blocker wie Propranolol oder Nadolol (cave: Hypotonie),
- Ängstlichkeit und Agitation: Phenothiazine (z. B. Chlorpromazin), ggf. Narkotika
- zerebrale (epileptische) Anfälle: Benzodiazepine, Gabapentin, und Vigabatrin
- Analgesie bei starken Schmerzen: z. B. Morphin (mögliche Atemdepression beachten).
(Informationen dieser Listen nicht unkontrolliert übernehmen!)
Verweise
- Akute intermittierende Porphyrie (AIP)
- Erythropoetische Protoporphyrie
- Kongenitale erythropoetische Porphyrie
- Porphyria cutanea tarda
- Chronische hepatische Porphyrie
- Porphyria variegata
- Delta-Aminolävolinsäure
- Bauchschmerzen
- Ernährung bei Lebererkrankungen
- Symptome bei Leberkrankheiten
- Laborwerte bei Leberkrankheiten
Verweise
- Rambam Maimonides Med J. 2018 Apr 19;9(2):e0013. doi: 10.5041/RMMJ.10333. [↩]
- Gastroenterology. 2019 Aug;157(2):365-381.e4. DOI: 10.1053/j.gastro.2019.04.050.[↩]
- Brain Behav. 2021 Nov;11(11):e2389. DOI: 10.1002/brb3.2389[↩]
- Metabolites. 2014 Nov 3;4(4):977-1006[↩]
- Am J Med. 2014 Nov 8. pii: S0002-9343(14)00967-X[↩]
- J Inherit Metab Dis. 2004;27(4):529-36[↩]
- J Intern Med 2000; 247: 407-409[↩]
- J Assoc Physicians India 2002; 50: 443-445[↩][↩]
- Alcohol Alcohol. 2000 Mar-Apr;35(2):109-25[↩]
- World J Gastroenterol. 2010 September 28; 16(36): 4526–4531[↩]
- Cancers (Basel). 2022 Jun 15;14(12):2947. DOI: 10.3390/cancers14122947[↩]
- Handb Clin Neurol. 2014;120:839-49[↩]
- Dermatol Clin. 2014 Jul;32(3):369-84[↩]
- Liver Int. 2012 Jul;32(6):880-93. doi: 10.1111/j.1478-3231.2012.02794.x[↩]
- Hepatology. 1998 Jan;27(1):181-4[↩]
- J Gastroenterol Hepatol. 2005; 20: 456-62[↩][↩]
- Neuropathology. 2007 Apr;27(2):133-8[↩]
- Prim Care Companion CNS Disord. 2011;13(6). pii: PCC.11br01234[↩]
- J Intern Med 1993; 234: 611-613[↩]
- N Engl J Med. 2020 Jun 11;382(24):2289-2301. doi: 10.1056/NEJMoa1913147[↩]
- Neuroradiology 1999; 41: 835-839[↩]
- Neuroradiology 2002; 44: 839-841[↩]
- Cell Mol Biol 2002; 48: 17-26[↩]
- Ann Clin Biochem. 2013 May;50(Pt 3):204-16[↩]
- N Engl J Med. 2019 Feb 7;380(6):549-558. doi: 10.1056/NEJMoa1807838[↩]
- N Engl J Med. 2020 Jun 11;382(24):2289-2301. DOI: 10.1056/NEJMoa1913147[↩]
- Expert Rev Clin Pharmacol. 2022 Apr;15(4):383-393. doi: 10.1080/17512433.2022.2075848.[↩]
- Pharmacol Res 2002; 45: 355-359[↩]
- Br J Nutr. 2010 Jan;103(1):69-76[↩]
- Endoscopy 2002; 34; 341-342[↩]
- Cancer Invest 2002; 20: 276-286[↩]
- Int J Biochem Cell Biol. 2002 May;34(5):544-53[↩]
- Semin Liver Dis 2005 Nov;25(4):461-72[↩]
- Front Neurol. 2022 Nov 21;13:1004125. DOI: 10.3389/fneur.2022.1004125.[↩]
- Hepatology. 2014 Sep;60(3):1082-9[↩]